①一种可燃性气体单质;
②一种难挥发的酸;
③一种常见金属氧化物;
④一种可溶性的盐。
根据国家标准《预包装特殊膳食用食品标签通则》,固体或液体食品中每100g或100mL的糖和脂肪含量低于或等于0.5g,即可标注 “零糖~零脂”:每100mL饮料的能量低于或等于17kJ,即可标注“零卡”,这些饮料的甜味剂通常是各种代糖,例如赤藓糖醇C4H10O4就是常见的填充型甜味剂,具有爽口的甜味,因其不被酶所降解,不参与糖代谢和血糖变化。医生建议多喝白开水、矿泉水为宜。根据上述信息,试回答:

①赤藓糖醇属于(选填“氧化物”,“无机物”或“有机物”之一)。
②赤藓糖醇分子中,碳、氢原子个数比为(填最简整数比),其所含元素质量分数最大的是(写元素符号)。
③饮料瓶通常是由聚丙烯塑料制成的,它属于材料。(选填“金属”,“无机非金属”,“有机合成”或“复合”之一)
④喝完饮料,废弃的饮料瓶应该投入垃圾箱(填序号)。
A.  B.
B.  C.
C.  D.
D. 
⑤下列关于碳酸饮料的说法中,错误的是(填序号)。
A.夏天天气炎热,可以随意饮用大量的冰镇碳酸饮料解暑降温
B.不锈钢保温杯不适合盛装碳酸饮料,因为它们之间会发生化学反应
C.喝了冰镇碳酸饮料易打嗝,因为CO2气体的溶解度随温度升高而变小
D.欲测定某碳酸饮料的酸性强弱,可选用湿润的pH试纸
“要把碳达峰,碳中和纳入生态文明建设整体布局。”“碳达峰”就是我们国家承诺在2030年前,二氧化碳的排放不再增长,达到峰值之后再慢慢减下去:而到2060年,针对排放的二氧化碳,要采取植树、节能减排等各种方式全部抵消按,这就是“碳中和”。

②能源的清洁低碳化,是“十四五”碳达峰部署的重点工作。页岩气是蕴藏于页岩层可供开采的天然气资源,其成分以甲烷为主,是一种清洁、高效的能源资源和化工原料,主要用于居民燃气、城市供热、发电、汽车燃料和化工生产等。
请写出甲烷在空气中完全燃烧的化学反应方程式:,该反应属于反应。(选填“化合”、“分解”、“氧化”或“复分解”之一)
②完善能源双控制度,构建以新能源为主体的新型电力系统。下列选项中,不属于新能源的是(填序号)。
A.氢能B.风能C.太阳能D.石油
③氢氧燃料电池汽车替代传统能源汽车,可有效减少碳排放。氢氧燃料电池供电的过程中,能转化为电能。
④实现碳达峰,碳中和是一场硬仗,需要每个人的努力与践行。下列做法中,不符合“低碳生活”的是(填序号)。
A.骑行共享单车,倡导绿色出行B.践行光盘行动,杜绝铺张浪费
C.旧衣焚烧掩埋,加快生产销售D.选用节能家电,减少能源消耗
如图所示为Na2CO3和NH4Cl两种物质的溶解度曲线。试回答下列问题:

①由图可知,t1℃时,两者中溶解度较大的物质是。
②t2℃时, NH4Cl饱和溶液的溶质质量分数Na2CO3饱和溶液的溶质质量分数。(选填“大于”、“小于”或“等于”)
③t1℃时,25g水中加入10 g Na2CO3固体,经充分搅拌后,所得溶液的质量为g。
④t2℃时,将等质量的NH4Cl饱和溶液和Na2CO3饱和溶液均降温至t1℃,析出晶体较多的是。
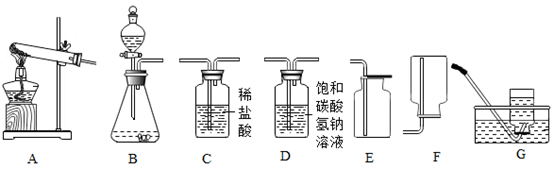
根据题目要求,回答下列问题:
(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①他所选仪器的连接顺序应为(填写仪器序号字母)。
②乙同学制取二氧化碳的化学反应方程式为。

①实验过程中,观察到装置C里的红棕色粉末变为黑色,其反应的化学方程式为。
②装置A的作用为。
③从绿色化学角度考虑,上述实验装置的不足之处是。
④实验前称取了10.0g该氧化铁样品放入装置C中,充分反应后,测得硬质玻璃管中剩余固体的质量为7.6g,则该样品中氧化铁的质量分数为(计算结果精确至0.1%)。

①物质A的化学式为。
②写出物质B与C发生反应的化学方程式:。

根据上述信息和分析推理,试回答下列问题:
①气体D的化学式为。
②无色溶液G中大量存在的阳离子是(写离子符号)。
③生成白色沉淀F的化学方程式为。
④固体混合物A中,还不能确定的物质是(写化学式)。
⑤白色沉淀B中,一定存在的物质是(写化学式),原因是。
![]()
(方案一)将二氧化氮通入水中,发生的反应为:
(方案二)将二氧化氮和氧气同时通入水中,其反应原理为:
上述方案中,更符合绿色化学理念的是方案(填“一”或“二”),理由是。

试计算:小颖所测硝酸溶液样品的溶质质量分数?(根据化学方程式计算,计算结果精确至0.1%)