一、选择题
-
1.
蛋白质可以维持人体的生长发育和组织更新,下列食物中富含蛋白质的是( )
A . 馒头
B . 豆制品
C . 植物油
D . 水
-
2.
下列所示变化中与其他三种变化有着本质不同的是( )
A . 火药爆炸
B . 衣服晒干
C . 纸张燃烧
D . 酒变酸
-
3.
下列物质的用途是利用其化学性质的是( )
A . 稀有气体用制霓虹灯
B . 金属铝质易拉罐
C . 碳酸氢钠用于焙制糕点
D . 铜线用于制导线
-
4.
下列关于空气的说法不正确的是( )
A . 洁净的空气是纯净物
B . 空气是一种重要的资源
C . 空气质量对于人类的生存至关重要
D . 植物的光合作用是空气中氧气的主要来源
-
A . 原子序数为12
B . 核外电子数为 24
C . 元素符合为Mg
D . 相对原子质量为24.31
-
6.
如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )

A . ②化合物③氧化物
B . ①单质、③含氧化合物
C . ①单质、③化合物
D . ②含氧化合物、④氧化物
-
7.
类比是化学学习的重要思想,下列说法正确的是( )
A . 铁、铝等金属能和稀酸反应,所以金属铜也能和稀酸反应
B . 稀盐酸、稀硫酸都能和碳酸盐反应,所以醋酸也能和碳酸盐反应
C . 水结冰后不再流动,所以结冰后水分子也不再运动
D . 食盐水能导电,食盐水是溶液,所以溶液都能导电
-
8.
Sb2O5是一种重要的阻燃剂,用X来表示生成该阻燃剂的化学方程式为:X+2H2O2=Sb2O5+2H2O,根据质量守恒定律推断X的化学式为( )
A . SbO2
B . Sb2O3
C . HSbO3
D . H3SbO4
-
9.
从分子或原子的角度分析并解释下列现象,其中正确的是( )
A . 搜救犬通过闻气味找到搜寻的目标——分子在不断运动
B . 温度计中的水银热胀冷缩——原子体积改变
C . 铜在空气中加热变黑——原子种类发生改变
D . 一氧化碳有毒,二氧化碳无毒——构成物质的分子相对分子质量不同
-
10.
(2016九上·东港期中)
苏州的“碧螺春”享誉全国.“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C
76H
52O
46 . 下列说法错误的是( )
A . 单宁酸由碳、氢、氧三种元素组成
B . 一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成
C . 单宁酸中碳、氧元素的质量比为57:23
D . 单宁酸中氢元素的质量分数最小
-
11.
等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属均显+2价),生成H
2的质量与反应时间的关系如图所示,下列说法不正确的是( )

A . 三种金属的活泼性:乙>甲>丙
B . 生成氢气的质量:甲>乙>丙
C . 相对原子质量:甲>乙>丙
D . 消耗硫酸的质量:甲>乙>丙
-
12.
如图是同学们利用大可乐瓶设计的储气装置(铁架台未画出),以下说法不正确的是( )
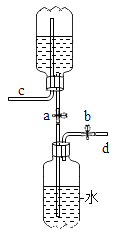
A . 打开止水夹a、b.气体从d管倒入储存在下面的瓶子里,水被压入上瓶
B . 取用气体时,可通过控制止水夹a、b,靠水的重力方便地将气体排出
C . 气体被储存在装置中,c导管也必须安装止水夹
D . 该装置也可用于实验室制取二氧化碳的发生装置
-
13.
化学在能源利用、环境保护等方面起着重要的作用。下列有关做法错误的是( )
A . 为治理雾霾,禁止使用化石燃料
B . 变废为宝,将地沟油转发为航空燃油
C . 城市道路使用太阳能景观灯,节能又环保
D . 用二氧化碳和水等合成新型燃油,有利于减缓温室效应
-
14.
下列做法,不正确的是( )
A . 用灼烧的方法区分羊毛和涤纶
B . 用肥皂水区分硬水和软水
C . 用品尝的方法区分糖水和火碱水
D . 用碘水区分奶粉和淀粉
-
-
-
17.
化学对人类的生活和社会发展做出了巨大的贡献。下列有关主题知识与应用不正确的是( )
选项 | 主题 | 知识与应用 |
A | 化学与生活 | 防治骨质疏松--服用钙片 |
B | 化学与能源 | 改善能源结构--开发太阳能、氢能 |
C | 化学与环境 | 减少白色污染--禁止使用塑料制品 |
D | 化学与安全 | 进入久未开启的菜窖--先做灯火试验 |
A . A
B . B
C . C
D . D
-
18.
A,B两种物质的溶解度曲线如图甲所示,在t
1℃时A、B两种物质配制溶液的情况如图乙所示。下列说法正确的是( )

A . t1℃时,两个烧杯内均有固体剩余,且质量相等
B . 由t1℃到t2℃的过程中,A溶液中溶质的质量分数减小
C . t2℃时,烧杯中的A溶液为饱和溶液
D . 由t2℃到 t1℃时,B的溶液中有晶体析出
-
19.
一些食物的近似pH如下表:
|
食 物
|
苹 果
|
葡 萄
|
牛 奶
|
玉米粥
|
|
pH
|
2.9-3.3
|
3.5-4.5
|
6.3-6.6
|
6.8-8.0
|
人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用上述食物中的( )
A . 苹果
B . 葡萄
C . 牛奶
D . 玉米粥
二、<b >填空题</b>
-
-
21.
初中化学学习中,我们初步认识了物质的微观结构。
-
(1)
氯化钠、金刚石、干冰三种物质中,由离子构成的物质是
-
(2)

是某粒子的结构示意图,该粒子在化学反应中容易
(填“得到”或“失去”)电子
-
(3)
下图是CO与O
2反应的微观示意图,反应前后没有发生变化的粒子是
(填序号)。

A . ①②
B . ②③
C . ③④
D . ④⑤
-
22.
化学与生活密切相关,请你用学过的知识回答下列问题:
-
-
-
(3)
以食叶为主的蔬菜,种植时应多施氮肥,请写出一种氮肥的化学式
-
-
(5)
甲醇CH3OH可用作赛车燃料。若其燃烧的产物与乙醇相同,则其燃烧的化学方程式是
-
23.
某钙片的标签如图所示

-
(1)
阅读上图,你认为该该片的主要功能是食用方法中“咀嚼后咽下”, “咀嚼”的目的是
-
(2)
你认为该该片除了它的主要功能外,还可以治疗。有人认为这种钙片食用量越多越好,你是否赞同,原因是
-
-
24.
下图是某化学反应的微观示意图。请结合图示回答下列为题:

-
-
-
(3)
在该反应的化学方程式中,A、C的计量数(即化学方程式中的系数)之比为
-
25.
下图是某课外活动小组的同学设计的实验室制取二氧化碳并检验其性质的装置示意图,请回答下列问题:

-
-
(2)
将A中产生的气体通入到B中一会儿,未见其中变浑浊。李祥同学认为这是浓盐酸挥发出的HCl气体干扰所致。他用化学方程式表示为:Ca(OH)2+CO2=CaCO3↓+H2O;CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 你的解释还可更简捷,请用一个化学方程式表示:;
-
(3)
张华同学用烧瓶收集A中产生的气体后,向其中加入过量无色透明的M溶液组成C装置,振荡,发现烧瓶中的气球逐渐变大,且溶液始终无色透明,则M可能是 (填写一种物质的化学式);
-
(4)
请设计一个方案,验证C装置中反应的生成物中含有CO32-。简述实验过程:
-
26.
同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液。
-
(1)
下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是 (填序号)
A . 氢氧化钠固体中含有不溶于水的杂质
B . 用水洗净后的烧杯未干燥就直接用于配制
C . 用量筒量取水的体积时采用俯视的方法读数
-
(2)
当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究。
[分 析] 氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式。
-
(3)
[猜想假设] 猜想一:该氢氧化钠样品部分变质。
猜想二:该氢氧化钠样品全部变质。
[查阅资料] ①已知反应:CaCl2 + Na2CO3 = 2NaCl + CaCO3↓
②部分盐酸溶液的pH如下表:
盐溶液 | CaCl2溶液 | Na2CO3溶液 | NaCl溶液 |
pH | 等于7 | 大于7 | 等于7 |
[进行实验] 请你与他们共同完成,并回答所给的问题:
实验步骤 | 实验现象 | 实验结论 |
步骤一:取少量样品于试管中, 加适量水振荡后全部溶解,滴 入CaCl2溶液至过量,充分反 应后,静置。 | 白色沉淀 | 样品中一定含有(填化学式) |
步骤一:取步骤一充分反应后 的少量上层清液于试管中,滴 入无色酚酞试液 |
| 结合两步实验得出 猜想一成立。 |
-
(4)
[拓展]研究性小组同学在步骤二中滴加的试剂除用指示剂外,还可以用替代。
-
三、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >探究题</b></p> </td> </tr> </table>
-
27.
质量守恒定律的发现对化学的发展做出了重要的贡献。

-
(1)
如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是(填序号),理由是
-
(2)
从微观角度分析有助于我们理解质量守恒定律.在一密闭容器内有4种物质A,B,C,D,它们在一定条件下发生化学反应.经过一段时间后停止反应,其中A,B,C,D的微观示意图和反应前后各物质的质量如下表所示.
物质 | A | B | C | D | 
|
微观示意图 | 
| 
| 
| 
|
反应前质量/g | 100 | 20 | x | 206 |
反应后质量/g | 32 | 140 | 126 | 46 |
(Ⅰ)从微观角度分析,化学反应中质量守恒的原因是.
(Ⅱ)B的化学式为.
(Ⅲ)该反应中B和C的质量比为.
(Ⅳ)表中x的值是.
-
28.
某兴趣小组在做完碳还原氧化铜实验后,进行了如图的探究:

-
(1)
[猜想]把氧化铜还原成铜的物质是:Ⅰ.石墨棒;Ⅱ..
-
(2)
[实验]用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹.按上述操作步骤实验,黑色粉末,那么猜想Ⅱ不成立.
-
(3)
[结论]石墨棒能使氧化铜还原成铜,该反应的化学方程式为.
-
(4)
[改进]把石墨棒换成铝粉,重复上述操作,又获成功.那么,称取等量的铝粉并进行同样的操作,其目的是
.改进后的实验证明,金属铝与铜活动性顺序是
,该反应的化学方程式为
.
[拓展]如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好.联想在空气中灼热的铁丝不能燃烧,而铁粉能燃烧,其原因是.
四、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >推断题</b></p> </td> </tr> </table>
-
29.
已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质。其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色,I是地壳中含量最高的元素所形成的常见气体单质,人体胃液中含有A,可以帮助消化。根据图所示转化关系,回答下列问题。(图中反应条件均已略去,反应物和生成物均已给出)

-
-
-
(3)
上图中涉及到 基本反应类型。
A . 一种
B . 二种
C . 三种
D . 四种
五、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >计算题</b></p> </td> </tr> </table>
-
30.
烧杯中装有一定量的盐酸和硫酸铜的混合溶液,已知该溶液中含有HCl的质量为3.65g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量如下表所示:

请回答下列问题:
-
-
(2)
参加反应的NaOH溶液的总质量是多少克?(结果保留小数点后面一位)



