一、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >选择题</b></p> </td> </tr> </table>
-
1.
Cr2O3可以用作某些化学反应的催化剂,其中Cr元素的化合价为 ( )
A . +2
B . +3
C . +5
D . +6
-
A . Ca(H2PO4)2
B . NH4NO3
C . K2SO4
D . NH4H2PO4
-
3.
有X、Y、R三种金属,将X和Y分别浸入盐酸中,Y溶解并产生氢气,X不反应,将X放入RSO4的溶液中,X表面有R析出,则三种金属活动性顺序是( )
A . R>X>Y
B . X>Y>R
C . R>Y>X
D . Y>X>R
-
4.
下列各组离子在溶液中可以大量共存的是( )
A . Ba2+、NH4+、NO3-、Cl-
B . H+、 K+、 HCO3-、NO3-
C . Ca2+、Ag+、CO32-、Cl-
D . Na+、Cu2+、SO42-、OH-
-
5.
茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等。下列有关茶氨酸的说法中正确的是( )
A . 茶氨酸属于有机高分子化合物
B . 茶氨酸中碳元素与氢元素的质量比为6︰1
C . 茶氨酸中氧元素的质量分数最大
D . 一个茶氨酸分子中含有一个氮分子
-
6.
已知某两种物质在光照条件下能发生化学反应,其微观示意图如下(说明:一种小球代表一种元素的原子)。则下列说法正确的是( )

A . 该反应属于置换反应
B . 图示中的反应物都是单质
C . 图示中共有4种分子
D . 该图示不符合质量守恒定律
-
7.
两种不含结晶水的晶体A,B的溶解度曲线如右图所示。下列分析正确的是( )
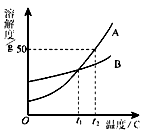
A . t1℃时,A,B两种物质的饱和溶液中溶质的质量相等
B . t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3
C . 将t1℃时,A,B两种物质的饱和溶液升温至t2℃,所得溶液的溶质质量分数的大小关系是A>B
D . 将B的不饱和溶液变为饱和溶液,可采用升温的方法
-
-
A . 蚕丝
B . 羊毛
C . 涤纶
D . 棉花
-
-
11.
下列粒子结构示意图中,表示阳离子的是( )
-
12.
除去下列物质中的少量杂质,方法错误的是( )
选项 | 物质 | 少量杂质 | 方 法 |
A | CO | CO2 | 通过足量的氢氧化钠溶液,干燥 |
B | Cu粉 | Fe粉 | 加入足量的稀硫酸,溶解,过滤,洗涤,干燥 |
C | CaO | CaCO3 | 加入适量的稀盐酸,溶解,过滤,洗涤,干燥 |
D | KCl溶液 | CuCl2 | 加入适量的氢氧化钾溶液,过滤 |
A . A
B . B
C . C
D . D
二、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >填空题</b></p> </td> </tr> </table>
-
13.
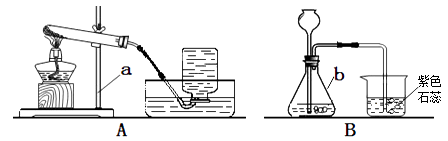
某化学兴趣小组利`用下列装置进行O
2、CO
2的实验室制法和有关性质的探究。
-
-
(2)
用氯酸钾和二氧化锰固体混合物来制取O2 , 应选用上图中的装置(填字母),其发生反应的化学方程式为。
-
(3)
①写出B装置中产生CO
2的化学方程式
。
②某同学用浓盐酸和大理石在B装置中反应,并检验 CO2的有关性质。此时观察到烧杯中紫色石蕊溶液变红,你对这一变化的合理解释有(填字母)。
A.产生的CO2直接使石蕊溶液变红
B.产生的CO2与水反应生成H2CO3使石蕊溶液变红
C.挥发出的氯化氢溶于水使石蕊溶液变红
-
(4)
若B中烧杯内盛有含氢氧化钙0.37 g的石灰水,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?(请写出计算过程)
-
14.
玄武湖是南京著名的淡水湖。某同学对玄武湖的水样进行了相关的探究。
-
(1)
澄清透明的玄武湖水属于(填“纯净物”或“混合物”)。
-
(2)
可以利用 (填字母)来测定湖水的酸碱度。
A . 酚酞溶液
B . 石蕊溶液
C . pH试纸
-
(3)
检验湖水是软水还是硬水,可向水样中加入,搅拌,观察现象。
-
-
15.
元素周期律和周期表是学习化学的重要工具。下表是元素周期表的部分信息。

-
-
(2)
从原子结构角度看,同一周期元素的原子具有相同的
数。某粒子结构示意图为

,该粒子所属元素位于周期表的第
周期。
-
(3)
观察硫原子结构示意图,在下图中填空:

-
16.
小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如下图:

-
-
-
(3)
在用托盘天平称取氯化钠的过程中,发现指针偏向分度盘右侧,他接下来的操作是。
-
(4)
如果小华配制的NaCl溶液的溶质质量分数小于20%,则造成此误差的可能原因有 。
A . 装入试剂瓶时,烧杯内残留少量液体
B . 量取水时仰视读数
C . 向烧杯中倒水时,有少量水溅出烧杯外
D . 称量纸上残留少量氯化钠
-
17.
能源的开发、储存和综合利用是世界各国科学家关注的重大课题。
-
(1)
现用的汽油、航空煤油、柴油等是根据沸点不同从石油中分馏出来,石油分馏的过程属(选填“物理”或“化学”)变化。化石燃料中主要含有碳、氢元素,还含有少量硫、氮等元素,燃烧时,这些元素常常转化为等气体污染物。
-
(2)
燃烧是化学能转化为热能的常见形式,下图A、B是关于燃烧条件探究的实验。
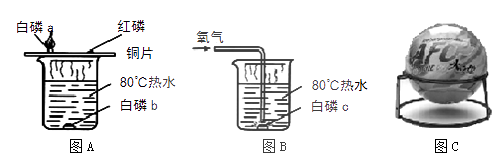
① 图A铜片上的白磷能燃烧,红磷不能燃烧,由此现象能得出的结论是。
②图B中发生反应的化学方式程为。
-
(3)
破坏燃烧条件可以灭火,避免火灾。
①上图C所示的“火立熄”接触到火焰3~5秒后炸开,释放的粉末覆盖在可燃物上,同时放出不可燃气体,使火焰熄灭。“火立熄”的灭火原理是(填序号)。
A.清除可燃物 B.使可燃物与氧气隔绝 C.降低可燃物的着火点
②CO2用于扑灭一般可燃物引起的火灾,利用了它的和密度比空气大的性质。
-
18.
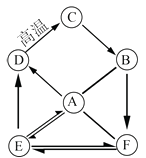
A,B,C,D,E,F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系。“→”表示物质间存在着相应的转化关系,“—”表示物质间能发生反应(部分反应物、生成物和反应条件未标出)。
请问答下列问题:
-
-
-
(3)
图示转化关系中未涉及到四种基本反应类型中的。
三、<table border=0 cellspacing=0 cellpadding=0 > <tr > <td valign=top > </td> <td > <p><b >探究题</b></p> </td> </tr> </table>
-
19.
某班化学实验课进行酸碱盐的性质实验。
〖实验一〗自制酸碱指示剂
-
(1)
取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色。分别装好待用。
取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图。

记录如下:
| NaOH溶液 | 稀盐酸 |
紫包菜汁液 | ①绿色 | ②红色 |
白菜汁液 | ③无色 | ④淡黄色 |
你认为两种汁液中,更适合做酸碱指示剂的是。
-
(2)
再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色。则苹果汁溶液显性。
-
(3)
〖实验二〗探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是;该反应的化学方程式为。
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为。
-
(4)
〖实验三〗废液再探究
〖实验二〗结束后,两组同学将全部的废液集中倒进一个废液缸中。兴趣小组同学对废液进行过滤,得到无色滤液。
【提出问题】
滤液中含有什么溶质?
【做出猜想】
滤液中一定含有,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种。
-
(5)
【实验探究】
①取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色。
②继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有。根据①②判断滤液中一定含有。
③为最终确定该滤液的组成,还需补充的实验是:,观察到白色沉淀。
-


