一、<h2 >选择题(本大题包括 15 个小题,每小题 3 分,共 45 分。在每小题列出的四个选项中,只有一个是正确的,请将答题卡上对应题目所选的选项涂黑)</h2>
-
1.
下列生产过程发生了物理变化的是( )
A . 烧制石湾公仔
B . 酿制石湾玉冰烧酒
C . 酿造海天酱油
D . 自来水厂过滤
-
2.
下列物质中含有氧分子的是( )
A . 高锰酸钾
B . 空气
C . 过氧化氢
D . 氯酸钾
-
-
4.
下列物质中属于空气污染物的是( )
A . 一氧化碳
B . 二氧化碳
C . 氧气
D . 氮气
-
5.
一走进南庄镇紫南村“阿农湾”农场就闻到阵阵瓜果香,合理的解释是( )
A . 分子数目变多
B . 分子在不断运动
C . 分子体积变大
D . 分子发生了分解
-
6.
下列物质的用途是利用其物理性质的是( )
A . 液氢做燃料
B . 氧气用于气割
C . 干冰做制冷剂
D . 氩气做保护气
-
-
8.
下列现象描述不正确的是( )
A . 硫在空气中燃烧发出微弱的淡蓝色火焰
B . 铁在氧气中燃烧生成一种黑色固体
C . 红磷在空气中燃烧产生大量白雾
D . 木炭在氧气中燃烧发出白光
-
9.
用下图所示的简易净水器处理浑浊的河水,下面分析正确的是( )

A . 净水器能杀菌消毒
B . 净水器不能将硬水变为软水
C . 小卵石和石英砂的位置调换对净水效果没有影响
D . 净化后的水是纯净物
-
10.
下列化学符号中数字“2”表示的意义,正确的是( )
A . SO2:表示二氧化硫中含有 2 个氧原子
B . 2Fe:表示 2 个铁原子
C .  :表示一个镁离子带 2 个单位正电荷
D . S2-:表示硫元素的化合价为﹣2 价
:表示一个镁离子带 2 个单位正电荷
D . S2-:表示硫元素的化合价为﹣2 价
-
11.
科学家用计算机模拟后确认,60 个 N 原子可结合成 N60 分子。下列关于 N60 的叙述中正确的是( )
A . N60 的相对分子质量为 840
B . 一个 N60 分子中含有 30 个 N2 分子
C . N60 是一种新型的化合物
D . N60 和 N2 的性质完全相同
-
12.
二氧化氮气体通入水中发生如下反应:3NO2+H2O=2HNO3+X,X 的化学式为( )
A . NO
B . N2O
C . N2O3
D . N2O5
-
13.
下列除去括号中的少量杂质的方法正确的是( )
A . CO2(CO)往集气瓶中伸入一根燃着的小木条
B . CO(CO2)把混合气体通过足量的澄清石灰水
C . CuO(C)把固体混合物隔绝空气加强热
D . N2(O2)往集气瓶中伸入一根燃着的小木条
-
14.
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,
下列说法正确的是( )
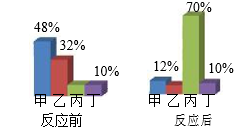
A . 丁一定是该反应的催化剂
B . 该反应中甲、丙的质量比为 1∶5
C . 该反应中乙、丙的质量比为 2∶5
D . 该反应一定是分解反应
-
15.
下图是已经所学物质之间的转化关系图,下列四种物质中可能是 C 物质的是( )
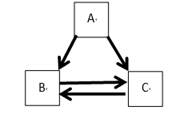
A . H2O2
B . Ca(OH)2
C . CaO
D . O2
二、填空题(本大题包括 2 小题,共 15 分。请把各题答案填写在答题卡上)
-
16.
-
(1)
从 C、H、O、Ca 四种元素中,选择适当元素,组成符合下列要求的物质,将其化.学.式.填在横线上:
① 溶于水中会放出大量的热的是;② 固体可用于人工降雨的是;
③“西气东输”的主要气体是;④ 用煤炉取暖时易发生中毒,主要是由于室内排放不畅引起的;⑤ 能作建筑材料石灰浆的是。
-
(2)
往变浑浊的澄清石灰水中持续通入二氧化碳气体,又会逐渐变为澄清透明的液体,原因是二氧化碳气体与水和碳酸钙反应生成可溶性的碳酸氢钙(Ca(HCO3)2),请用化学方程式表示这一变化过程并注明基本反应类型是:。
-
17.
锂元素在元素周期表中的某些信息如图甲所示,锂原子与另外三种粒子的结构示意图如图乙所示。

-
-
-
(3)
锂原子与图乙中(填“A”“B”或“C”)粒子的化学性质相似。
-
(4)
图乙中由 A 和
B 两粒子构成的物质的化.学.式.是。
-
(5)
图丙是工业上生产尿素[化学式:CO(NH2)2]的反应的微观示意图。
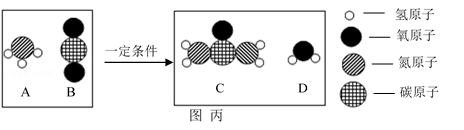
写出该反应的化学方程式为。
三、实验题(本大题包括 2 小题,共 20 分。请把各题答案填写在答题卡上)
-
18.
选择下列仪器进行氧气制取和有关性质的实验,并回答有关问题。

-
-
(2)
实验室用高锰酸钾制取氧气,反应的化学方程式为;组装发生和收集装置时应选择上述仪器中的①③(填序号),还需补充的一种仪器是,为防止冷凝水回流炸裂该仪器,正确固定该仪器的方法是。
-
(3)
某同学选择②⑦⑧组合实验室制取 CO2 的发生装置,该反应的化学方程式为。该发生装置的优点是,应该往锥形瓶中装入。
-
19.
某小组利用下图装置完成 O
2、 CO 或 CO
2 的有关实验, 实验过程中,他们从 a 处通入一种气体, 在 b 处放入一种固体。C 处放入一种溶液。

-
(1)
若从 a 处通入O2 , 观察到 b 处发出白光,c 处的无色溶液变浑浊,则 b 处放置的黑色固体为,c 处发生反应的化学方程式为。
-
(2)
若 b 处固体由红色变为黑色,且反应后的固体可被磁铁吸引,c 处紫色溶液变红。则 b 处发生反应的化学方程式为,d 处酒精灯的作用是。
-
(3)
若 b 处固体由红色变为黑色,b 处反应后的固体不能被磁铁吸引,c 处澄清石灰水不变浑浊。则 b 处发生反应的化学方程式为。
-
(4)
若 b 处固体由黑色变为红色,b 处反应后的固体不能被磁铁吸引,c 处澄清石灰水变浑浊。则 b 处发生反应的化学方程式为。
四、<h2 >综合能力题(本大题包括 1 小题,共 10 分)</h2>
-
20.
二氧化锰和硫酸铜溶液对过氧化氢的分解都有催化作用。为比较二者的催化效果,化学兴趣小组对此进行了探究。
-
(1)
【重温教材】
实验室可用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式为。二氧化锰是这个反应的催化剂,催化剂是指在化学反应里能其他物质的化学反应速率,而本身的和在化学反应前后都没有发生变化的物质。
-
(2)
【进行实验】
如图 1 所示实验:将 68g 5%的过氧化氢溶液快速推入锥形瓶中(装置气密性良好),并用数字化实验设备测定容器中的压强变化,结果如图 2 所示。
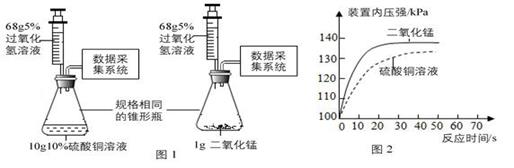
图 1 装置(不含数据采集系统)气密性检查的方法是夹住(或堵住)右侧导管口,向外拉注射器的活塞,一段时间后,松开手,注射器的活塞,则装置的气密性良好。
-
(3)
由图像可知:常温下,对过氧化氢的分解催化效果更好。
-
(4)
小明推测两条曲线最终将基本合并在一起,其理由是。
-
(5)
【反思拓展】
小强认为上述实验还不够严密,其理由是(写出一条即可), 由此可见在进行对比对照实验时应该要。
五、<h2 >计算题(本大题包括 1 小题,共 10 分)</h2>
-
21.
-
(1)
某加碘低钠盐的标签部分说明如图所示。

①碘酸钾(KIO3)中各元素的原子个数比为。
②碘酸钾(KIO3)碘元素的质量分数为。
③若该低钠盐中碘元素含量为 25mg/kg,中国营养学会推荐成年人每天摄入碘的量为 0.15mg,若其中 90%来源于食盐,则每天食用该碘盐的质量是g。
-
(2)
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品 20g,把 100g 稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应)。请计算:
|
序号
|
加入稀盐酸的质量/g
|
剩余固体的质量/g
|
|
第一次
|
25
|
14
|
|
第二次
|
25
|
8
|
|
第三次
|
25
|
5
|
|
第四次
|
25
|
n
|
表中 n 的数值为。
-
(3)
求完全反应后生成的二氧化碳的质量是多少?(写出计算过程,精确到 0.1)


