 钻石(C)
B .
钻石(C)
B .  水晶(SiO2)
C .
水晶(SiO2)
C .  食盐(NaCl)
D .
食盐(NaCl)
D .  钟乳石(CaCO3)
钟乳石(CaCO3)

 B .
B .  C .
C .  D .
D . 
地球村的“碳”危机,展示人类过度开发、高碳排放所造成的恶果,如温室气体产生的温室效应。二氧化碳、氧化亚氮(N2O)、甲烷和臭氧(O3)是地球大气中主要的温室气体,其中甲烷的化学式为。
A少买不必要的衣服
B使用节能电器
C洗碗时不间断地放水冲洗
D少开私家车,多乘公共交通工具
下列说法中,正确的是。
A钠可能与水反应
B钠的熔点比铁的熔点低
C维生素 A 中一定含有钠元素

(资料)①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
|
温度/℃ |
0 |
10 |
20 |
30 |
50 |
|
|
溶解度/g |
Ca(OH)2 |
0.18 |
0.17 |
0.16 |
0.15 |
0.14 |
|
K2CO3 |
107 |
109 |
110 |
114 |
121 |
|
|
KOH |
97 |
103 |
112 |
126 |
140 |
|
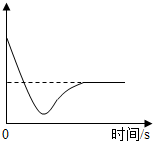
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
|
实验序号 |
① |
② |
③ |
④ |
|
加入氯化钠的质量/g |
9 |
36 |
81 |
90 |
|
溶液质量/g |
209 |
236 |
272 |
272 |
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是g。关于上述实验的叙述正确的是(填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体


①从微粒的角度说明图 B 反应的实质是。
②图 C 所示反应中,发生有效的相互作用而促使反应发生的微粒是(写出微粒的符号)。

下列说法正确的是(填数字序号)。
①该反应类型为复分解反应
② 4 种物质中属于氧化物的是 D
③反应前后,元素化合价均未发生变化
④若 48 gB 完全反应,则生成 C 的质量为 28 g

a处可观察到的现象是;b处点燃酒精灯的目的是。

①若 b 点表示的溶液中只含一种溶质,则 a 点表示的溶液中的溶质可能是(写出 1 种情况即可),从 a 点到 b 点的过程中,反应的化学方程式是。
②若从 b 点到 c 点的过程中,溶液的质量不断增加,则加入的另一种金属是。

① 在A装置的锥形瓶中加入大理石,向长颈漏斗中注入稀盐酸,A中反应的化学方程式为。
② 连接A、B装置,打开a、c,关闭b,向B中集气瓶内充入气体,检验集气瓶中气体已收集满的方法是。
③ 关闭a、c,打开b,用冷毛巾捂住B中集气瓶,一段时间后,观察到B装置中的现象是, B中反应的化学方程式为。
(资料)氯化氢气体和氨气均极易溶于水,且两者反应生成白色固体氯化铵(NH4Cl)。
在c右端的导管口套一个气球,在A的锥形瓶中放入浓盐酸,向长颈漏斗中注入浓硫酸,有HCl气体产生,待A中的空气被排净后,连接A、B装置,打开a、c,关闭b,气球微微鼓起。产生HCl气体的原因是。
② 关闭a,将A中的药品替换为NaOH固体和浓氨水,待A中的空气被排净后,连接A、B装置,打开a,一段时间后关闭a,B中集气瓶内有白烟产生。冷却至室温后气球恢复原状。关闭c打开b,B中导管内的液面无任何变化。产生上述现象的原因是。
(查阅资料)①碱石灰是氧化钙、氢氧化钠的固体混合物。
②氯化钙溶液呈中性。
③CaCl2 + Na2CO3 = CaCO3 ↓+ 2NaCl
(进行猜想)久置碱石灰样品中可能含有 CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3 中的两种或两种以上成分。上述五种物质中,属于碱的是。样品中可能含有 Ca(OH)2 的原因是(请用化学方程式表示)。


试回答下列问题:
操作①的名称是。
A样品中加水后容器壁发热,说明样品中一定含有 CaO
B样品加足量水后仍有固体,说明样品中一定含有 CaCO3
C溶液 A 加入 CaCl2 溶液后产生固体,说明样品中一定含有 Na2CO3
D溶液 C 加入酚酞变红,说明样品中一定含有 NaOH