 B . 测溶液的pH
B . 测溶液的pH 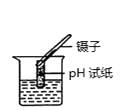 C . 稀释浓硫酸
C . 稀释浓硫酸 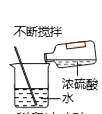 D . 蒸发食盐水
D . 蒸发食盐水 
【提出问题】A,B,C,D分别是什么溶液?
【实验药品】失去标签的四瓶溶液和无色酚酞试液
【实验仪器】试管、胶头滴管、烧杯等.
实验操作 | 实验现象 | 实验结论 |
①取四种溶液各少量于试管中,然后A与B、C与D溶液两两混合 | A、B混合产生大量气泡,C,D混合无明显现象 | A、B分别是溶液中的一种. C,D分别是溶液中的一种 |
②取四种溶液各少量于试管中,然后A与C,B与D溶液两两混合 | A、C混合产生白色沉淀,B,D混合无明显现象 | A为溶液;C为溶液;由此区分出B、D溶液 |
【继续探究】
将四种溶液各少量倒入一洁净的烧杯中,再滴入几滴无色酚酞试液,充分反应静置后发现,烧杯底部有白色沉淀,上层清液为无色.则上层清液中一定含有的溶质是(指示剂除外),可能含有的溶质是为验证可能含有的溶质是否存在,应补充的实验设计是.

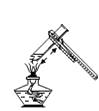
①按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样品,称得装置和药品的总质量为564.57g;
②在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
③旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
④反应结束后,称得装置及装置内所有物质的总质量为570.57g
请根据上述实验回答下列问题: