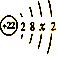 ,其中x=;
,其中x=;

【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质.
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2;猜想2.CO和H2O.


【提出猜想】猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠
【查阅资料】①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解
实验操作 | 实验现象 | 实验结论 | |
小月 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH7(填“>”、“<”或“=”) | 溶液呈碱性,猜想1成立 |
小妮 | 用如图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变浑浊 | 猜想2成立,试管B中反应的化学方程式为. |
①小月实验结论不准确的原因是;
②小妮的实验方案不能排除白色粉末是否含有.
【结论分析】探究后他们核查到添加剂的成分是柠檬酸和碳酸氧钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的.