
①请从上表中查出关于硫元素的一条信息:.
②Ar的相对原子质量为.
③第12号元素与第17号元素组成的化合物是(填写化学式)
④在元素周期表中,同一族(纵行)的元素由于最外层电子数相同所以具有相似的化学性质,则下列各组元素具有相似化学性质的是(填序号)、
A.C和Ne B.B和Mg C.Al和Si D.F和Cl
①当a=时,该粒子是原子.
②当a=9时,该粒子是(选填“原子”“阳离子”“阴离子”之一)
③当a=时,该粒子是带有3个单位正电荷的阳离子,其离子符号为.
①潮汐能 ②生物能 ③太阳能 ④化学能
![]()
通过过程②可得到碳酸氢钠,化学方程式为NaCl+NH4HCO3═NaHCO3+X.请写出X的化学式,此反应属于反应(选填”化合””分解“”复分解“”氧化“”置换“之一)
①t2℃时,A的溶解度为.图中P点的意义为.
②t2℃时,AB饱和溶液溶质的质量分数为AB.(选填“>”“=”“<”之一)
③将A和B的饱和溶液分别由t2℃降温到t1℃时(假设溶剂质量不变).请判断它们溶液中溶质的质量分数如何变化?简要写出理由.

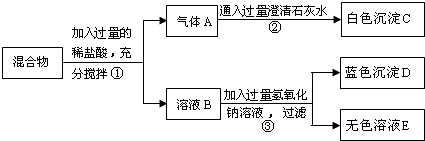
试根据实验过程和发生的现象填写以下空白: