 拉瓦锡
B .
拉瓦锡
B .  卢瑟福
C .
卢瑟福
C .  门捷列夫
D .
门捷列夫
D .  道尔顿
道尔顿
 可乐
C .
可乐
C .  豆浆
豆浆
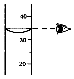 读液体体积
B .
读液体体积
B .  加热液体
C .
加热液体
C . 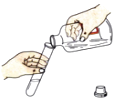 倾倒液体
D .
倾倒液体
D .  取用固体
取用固体
食品添加剂
食品添加剂指在生产食品的过程中,在食品中加入的化学物质。
食品添加剂一般不单独作为食品来食用;它可以是天然物质,也可以是人工合成的物质;把它加入到食品中是为了改善食品的色、香、味,同时也能起到防腐、保鲜的作用。
到目前为止,全世界食品添加剂品种达到25000种,它们都可以食用。但是,像三聚氰胺、孔雀石绿、苏丹红等物质却禁止在食品中添加,因为它们是化工原料。
我国《食品添加剂使用卫生标准》中规定了各类食品中食品添加剂的安全用量。如作为甜味剂的“甜蜜素”,其使用范围及最大使用量如下表所示。
使用范围 | 最大使用量(g/kg) |
酱菜、调味酱汁、糕点、冰淇淋、饮料等 | 0.65 |
蜜饯 | 1.0 |
陈皮、话梅、话李、杨梅干等 | 8.0 |
甜蜜素(C6H11NHSO3Na)是白色固体,味甜,外观与蔗糖相似,甜度为蔗糖的40~50倍,是一种常见的食品添加剂,被广泛应用于食品加工行业,其熔点是265℃,分解温度约280℃,无明显现象。蔗糖的熔点是186℃,在190—220℃的较高温度下,蔗糖发生反应,最终形成黑色物质。
目前,97%的食品中使用了各种添加剂,可以说,食品添加剂已成为现代食品工业生产中不可缺少的物质。
A.只选择不含食品添加剂的食品
B.关注食品营养表中添加剂的品种和用量
C.选择加工度低的食品,以免摄入过多的添加剂
D.只关注食品的营养成分,不在乎是否含有添加剂
A.需要的理由是。
B.不需要的理由是。

同学们感到很惊讶,于是展开探究。
【提出问题】棉花为什么会发生燃烧?
①过氧化钠与水反应生成氢氧化钠、氧气。
②过氧化钠与水反应生成氢氧化钠和气。
③过氧化钠与水反应放出大量热。
编 号 | 主要实验操作 | 实验现象 | 实验结论 |
打开装置中分液漏斗的活塞,滴加适量水后,关闭活塞。 | |||
将带火星的木条接近P处 | B瓶中有气泡产生;带 火星的木条复燃 | ||
③ | 过氧化钠与水反应放 出大量热 |
①同学们设计实验时,增加了防止发生爆炸的装置B,其原因是。
②经测定,过氧化钠与水反应还有氢氧化钠生成,该反应的化学方程式为。
③将少量水滴到包有Na2O2固体的棉花上,棉花团剧烈燃烧起来的原因是。