单选题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项符合题意。
- A、 有利于实现碳中和
- B、 有利于降低火炬燃料成本
- C、 有利于燃料充分燃烧
- D、 使开幕式点火场面更壮观
- A、 Na的结构示意图为
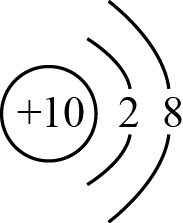
- B、 Na2O2既含离子键又含共价键
- C、 H2O2的电子式为

- D、 H2O属于非电解质
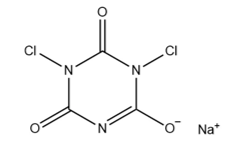
- A、 电负性:χ(N) > χ(O)
- B、 键极性:C-N > C-O
- C、 第一电离能:I1(C) > I1(N)
- D、 离子半径:r(O2-) > r(Na+)
|
|
|
|
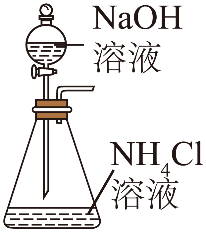
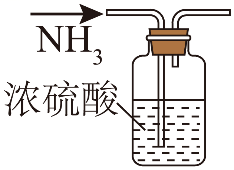
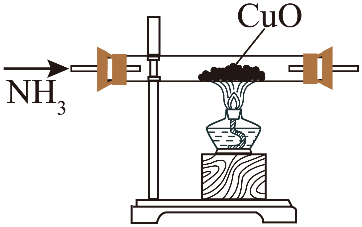
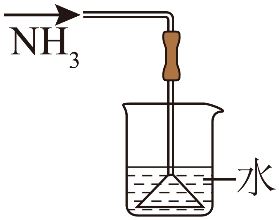
A.制取NH3 | B.干燥NH3 | C.验证氨气的还原性 | D.吸收尾气 |
- A、 A
- B、 B
- C、 C
- D、 D
周期表中ⅢA族元素(5B、13Al、31Ga、49In等)的单质及其化合物应用广泛。BF3极易水解,生成HBF4(HBF4在水中完全电离为H+和BF4-)和硼酸(H3BO3)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下Al2O3和焦炭在氯气的氛围中获得AlCl3。GaN的结构与晶体硅类似,是第三代半导体研究的热点。铟(In)主要用于生产液晶显示器和平板屏幕。
- A、 该反应的平衡常数
- B、 该反应一定能自发进行
- C、 该反应中每消耗1molNO2 , 转移电子的数目约为3.01×1023
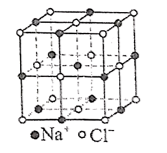
- D、 NaCl晶胞(如图所示)中每个Na+周围与其距离最近的Na+有6个
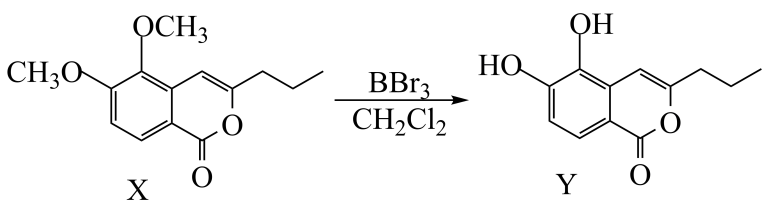
- A、 X中所有碳原子不可能共平面
- B、 Y与足量H2加成后有5个手性碳原子
- C、 1molY最多能与4molNaOH反应
- D、 1molY与浓溴水反应,最多消耗2molBr2
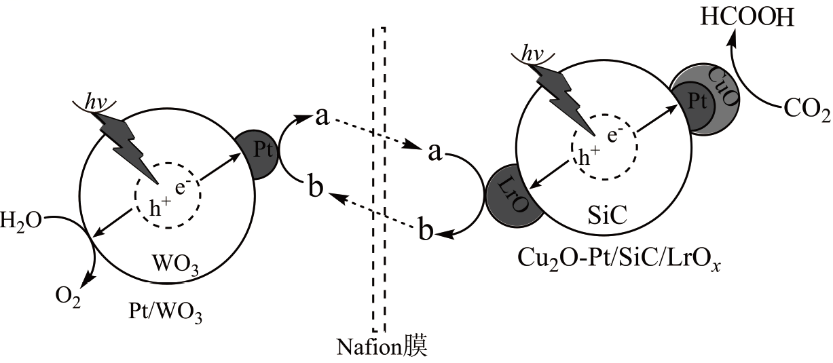
- A、 该反应能量转化形式为光能→化学能
- B、 该人工光合体系的总反应为2CO2+2H2O
2HCOOH+O2
- C、 图中a、b分别代表Fe3+、Fe2+
- D、 Cu2O-Pt上发生的反应为CO2 + 2e- + 2H+ = HCOOH
选项 | 实验探究方案 | 探究目的 |
A | 向Fe(NO3)2和KSCN的混合溶液中滴入稀硫酸 | 氧化性:Fe3+>H+ |
B | SO2通入酸性KMnO4溶液中 | SO2具有漂白性 |
C | 向试管中加入2mL5% H2O2和1mL2%CuSO4溶液,观察气泡产生情况 | Cu2+可促进H2O2分解 |
D | 向新制氯水中加入NaHCO3固体 | 氯水呈酸性 |
- A、 A
- B、 B
- C、 C
- D、 D
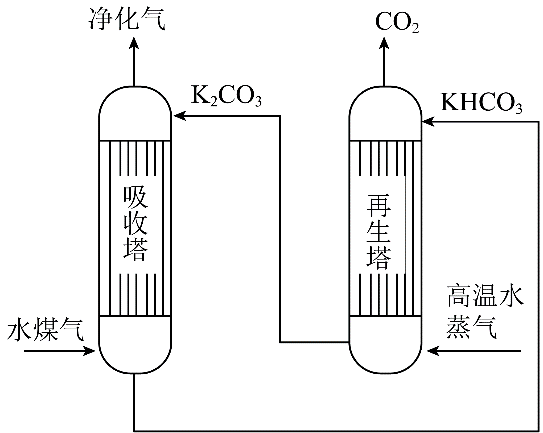
- A、 K2CO3溶液中:2c(K+) = c(CO32-) + c(HCO3-) + c(H2CO3)
- B、 吸收塔中c(CO32-) :c(HCO3-)=1:2时,溶液pH=10
- C、 再生塔所得到的溶液中可能存在:c(H2CO3)>c(HCO3-)
- D、 再生塔中发生反应的化学方程式:KHCO3 + KOH = K2CO3 + H2O + CO2↑
已知:Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41 kJ·mol-l
Ⅱ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=-165 kJ·mol-1
在两种不同催化剂作用下反应相同时间,CO2转化率和生成CH4选择性随温度变化关
系如图所示(CH4选择性=×100%)。
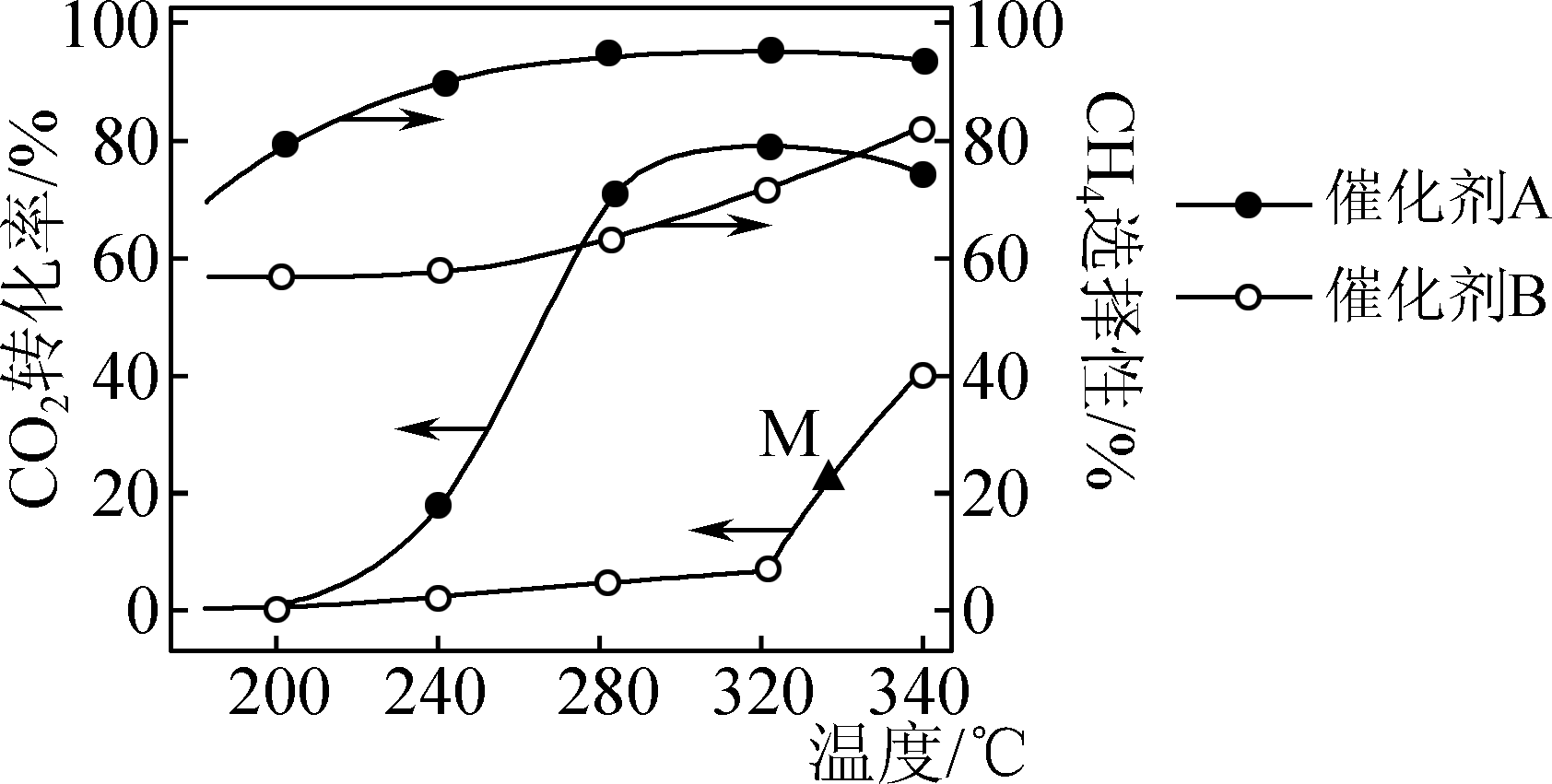
下列说法不正确的是( )
- A、 反应CO(g)+3H2(g)=CH4(g)+H2O(g)的ΔH=-206 kJ·mol-1
- B、 在280 ℃条件下反应制取CH4 , 选择催化剂A的效果较好
- C、 260~300 ℃间,使用催化剂A或B,升高温度时CH4的产率都增大
- D、 M点可能是该温度下的平衡点,延长反应时间,不一定能提高CH4的产率
非选择题:本题包括4小题,共61分。
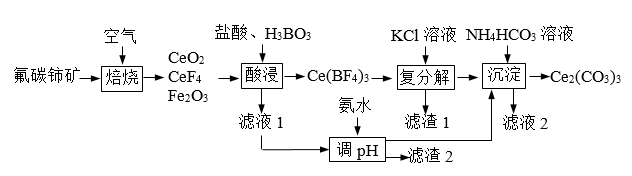
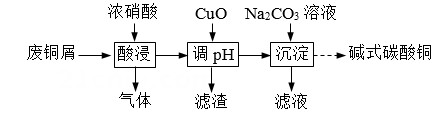
已知部分氢氧化物开始沉淀与沉淀完全的pH见下表:
物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 |
开始沉淀pH | 1.9 | 6.5 | 4.2 | 3.4 |
沉淀完全pH | 3.2 | 9.7 | 6.7 | 4.0 |
反应1:CO2(g) + 3H2(g)CH3OH(g) + H2O(g) ΔH1= - 49.5 kJ/mol
反应2:CO2(g) + H2(g)CO(g) + H2O(g) ΔH2= + 41.2 kJ/mol