单选题
试题详情
下表是氯化钠和硝酸钾的溶解度表,下列叙述中,错误的是( )
氯化钠和硝酸钾在不同温度下的溶解度
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| 氯化钠(克) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 硝酸钾(克) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
- A、 氯化钠和硝酸钾的溶解度随温度的升高而增大
- B、 在20℃时,要溶解36克氯化钠至少需要100克水
- C、 若硝酸钾中混有少量的氯化钠,可采用冷却热饱和溶液的方法来提纯硝酸钾
- D、 将80℃的氯化钠饱和溶液和80℃的硝酸钾饱和溶液各100克降温至20℃,析出晶体的质量分别是2.4克和137.4克
试题详情
20℃时,将45g氯化钠均分成五份,依次加入到盛有100g水的烧杯中,充分溶解。实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 氯化钠质量/g | 9 | 18 | 27 | 36 | 45 |
| 溶液质量/g | 109 | 118 | 127 | 136 | 136 |
下列分析正确的是( )
- A、 实验③所得溶液的溶质质量分数最大
- B、 实验④所得溶液是氯化钠的不饱和溶液
- C、 20℃时,氯化钠的溶解度为36g/100g水
- D、 将实验①所得溶液蒸发50g水,冷却到20℃,溶液达到饱和
试题详情
已知(1)20℃时,溶解度在10克以上的物质称为易溶物质,溶解度在1~10克的物质为可溶物质,溶解度在0.01~1克为微溶物质,溶解度小于0.01克的物质为难溶物质。(2)20℃时几种物质的溶解度如下:
| 物质名称 | 氯化钠 | 氢氧化钙 | 氯酸钾 | 硝酸钾 |
| 溶解度(克) | 36.0 | 0.165 | 7.4 | 31.6 |
下列说法正确的是( )
- A、 20℃时氢氧化钙是难溶物质
- B、 20℃时可以配制出20%的硝酸钾溶液
- C、 20℃时氯酸钾是易溶物质
- D、 20℃时硝酸钾的溶解度比氯化钠大
试题详情
日本政府拟将核污水排入太平洋的计划引起了全球关注。若该计划实施,不仅会导致海洋污染,某些污染物还可能通过水循环环节进入到大气,从而造成大气污染。下列水循环环节中,与污染物进入大气密切相关的是( )
- A、 降水
- B、 下渗
- C、 蒸发
- D、 径流
试题详情
20℃时,取一定质量的固体硝酸钾于烧杯中,把100克水平均分成四份依次加入烧杯,不断搅拌,使之充分到溶解,实验过程如图所示。下列分析正确的是( )

- A、 甲烧杯中,硝酸钾溶液是不饱和溶液
- B、 丁烧杯中,硝酸钾溶液是不饱和溶液
- C、 乙→丙过程中,硝酸钾溶液的溶质质量分数变大
- D、 丙→丁过程中,硝酸钾溶液的溶质质量分数变大
试题详情
一杯热硝酸钾溶液放在桌面上,一段时间后观察到烧杯底部有少量的晶体析出,如图所示。忽略水的蒸发,下列关于硝酸钾及其溶液的分析正确的是( )
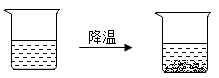
- A、 溶液质量不变
- B、 溶液的溶质质量分数变小
- C、 硝酸钾的溶解度变大
- D、 原溶液一定是饱和溶液
试题详情
现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示。下列判断正确的是( )
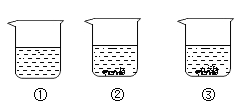
- A、 ①中所得溶液一定是不饱和溶液
- B、 ②③中所得溶液溶质的质量分数相等
- C、 若②中溶液升温到30℃,溶液的质量一定不变
- D、 若③中溶液恒温蒸发,溶质的质量分数一定变大
试题详情
人类的生产和生活都离不开水,地球上的水通过水循环不断地被利用。下列描述正确的是( )

- A、 水循环的环节只有蒸发、凝结和降水
- B、 海洋水可以通过水循环转化为湖泊水
- C、 地表径流水量一定与植物蒸腾量相等
- D、 人类直接利用最多的水资源是海洋水
试题详情
某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )
- A、 变大 不变
- B、 变大 变小
- C、 不变 变大
- D、 不变 不变
试题详情
小金在配硝酸钾溶液时得到下表数据,据此分析以下说法正确的是( )
| 序号 | 温度/℃ | 水的质量/克 | 加入硝酸钾的质量/克 | 所得溶液的质量/克 |
| ① | 10 | 100 | 40 | 120.9 |
| ② | 60 | 100 | 40 | 140 |
- A、 10℃时硝酸钾的溶解度为40克
- B、 ②所得溶液一定是60℃时硝酸钾的饱和溶液
- C、 若通过加热将①中剩余硝酸钾全部溶解,则溶液的溶质质量分数与加热前保持一致
- D、 若将②所得溶液降温至10℃,则溶液的溶质质量分数会变小
试题详情
某容器中装有盐水若干,老师让小科倒入质量分数1%的盐水100克以配成质量分数2%的盐水,但小科却错误的倒入100克水,老师发现后说你再将第三种盐水40克倒入水中就可得到2%的盐水了,那么第三种盐水的质量分数为( )
- A、 2.5%
- B、 4.5%
- C、 5%
- D、 7%
试题详情
如图所示为蒸发氯化钠溶液的过程,其中①→②一③为恒温过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,可以作出的正确判断是( )

- A、 在①→②过程中,氯化钠的质量分数保持不变
- B、 在②→③过程中,氯化钠的溶解度不断增大
- C、 在③→④过程中,水的质量分数不断增大
- D、 在②→④过程中,氯化钠的质量分数先不变后增大
试题详情
如图是教材中用来表示电解水过程的示意图(其中“  )分析示意图,可作出的正确判断是( )
)分析示意图,可作出的正确判断是( )

- A、 常温常压下水可以发生分解反应
- B、 电解水的最终产物是H、O原子
- C、 H原子是图示微粒中的最小微粒
- D、 O原子只有在通电条件下才能转化为O2分子
试题详情
20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。对所得溶液的有关说法错误的是( )
- A、 该溶液是饱和溶液
- B、 溶液中Na=和Cl-个数一定相等
- C、 溶液质量为100克
- D、 溶质与溶剂质量比为9:25
试题详情
20℃时,四个实验小组分别取不同质量的NaCl,逐渐加入到各盛有50g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。记录数据如下表:
实验小组 | 第一组 | 第二组 | 第三组 | 第四组 |
水的质量/g | 50 | 50 | 50 | 50 |
所取NaCl的质量/g | 15 | 20 | 25 | 30 |
剩余NaCl的质量/g | 0 | 2 | 7 | 12 |
下列说法错误的是( )
- A、 20℃时,50gNaCl饱和溶液中含有18gNaCl
- B、 用蒸发的方法可以使不饱和溶液变成饱和溶液
- C、 第二组所得溶液的溶质与溶剂的质量比为9:25
- D、 相同温度下,NaCl在水里的溶解度与水的质量无关
试题详情
下列操作均在室温下进行,且不考虑水分的蒸发。则溶液中溶质的溶解度和溶质质量分数都发生变化的是( )
- A、 将一定量硝酸钾不饱和溶液升温 10℃
- B、 将一定量饱和石灰水升温 10℃
- C、 取一定量蔗糖不饱和溶液向其中加入少量蔗糖
- D、 取一定量氯化钠饱和溶液向其中加入少量水
试题详情
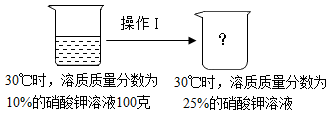
硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
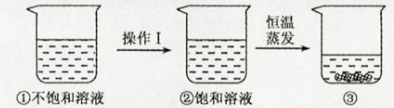
- A、 操作Ⅰ一定是降温
- B、 ①与②的溶液质量一定相等
- C、 ①与③的溶质质量一定相等
- D、 ②与③的溶质质量分数一定相等
试题详情
2018年5月,台州南部湾区引水工程开工,以级解台州雨部地区的用水紧张状况。该工程通过管道,将台州北部水资源向南部输送。该工程改变的水循环环节是( )
- A、 降水
- B、 地表径流
- C、 海水蒸发
- D、 水汽输送
试题详情
某“天气瓶"通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是( )

- A、 甲、乙
- B、 甲、丙
- C、 乙、丙
- D、 甲、乙、丙
试题详情
20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )
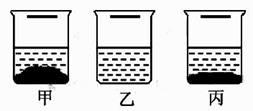
- A、 所得溶液可能都是饱和溶液
- B、 20℃时,乙溶液的溶质质量最小
- C、 溶液溶质的质量分数:甲>丙>乙
- D、 升高温度,溶液溶质的质量分数一定变大
填空题
试题详情
学习《物质的溶解》时小科同学进行了如下实验:往A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入50g、25g、5g同种固体物质,充分溶解后,静置,现象如图所示。

回答下列问题:
试题详情
下表是氢氧化钠溶液的密度与其质量分数对照表(20℃)。回答下列问题:
| 质量分数(%) | 10 | 20 | 30 | 40 | 50 |
| 密度(克/厘米3) | 1.11 | 1.22 | 1.33 | 1.43 | 1.53 |
试题详情
常温下,取100克质量分数为5%的NaCl溶液,先按实验1将NaCl溶液分成两等份,再进行实验2操作,如图所示。

完成下列问题:
试题详情
物质的溶解度不同,用途也不同。请据表回答:
表一 物质的溶解度(20℃)
| 物质 | NaOH | Ca(OH)2 | CaCO3 | CaSO3 |
| 溶解度(克) | 109 | 0.165 | 0.0014 | 0.0043 |
表二物质在水中的溶解性等级
| 200C时的溶解度(克) | >10 | 1-10 | 0.01-1 | <0.01 |
| 等级 | 易溶 | 可溶 | 微溶 | 难溶 |
试题详情
台州甘蔗制糖有着悠久的历史。甘蔗制糖的部分环节为:清洗甘蔗→压榨甘蔗→分离渣汁 →蒸发浓缩→……

试题详情
水循环是指地球上不同水体进行水分交换的过程。通过水循环,地球上的水、大气、岩石和生物发生了密切的联系。
试题详情
水的循环示意图中,序号①②③④表示水循环的主要环节(如图),据图完成下列问题:
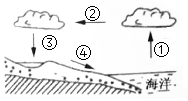
试题详情
下表是A、B、C三种固体物质在不同温度下(t1<t2<t3)的溶解度,请回答:
| 温度(℃) | t1 | t2 | t3 |
| 物质A(克) | 36.0 | 36.2 | 37.3 |
| 物质B(克) | 31.6 | 36.2 | 110.0 |
| 物质C(克) | 0.165 | 0.135 | 0.076 |
试题详情
甲烧杯中盛有30℃、溶质质量分数为20%的饱和硫酸铜溶液100克,进行如图所示实验(不考虑水分蒸发)。

实验探究题
试题详情
为了解决人们在野外生活和工作时的饮水问题,小金开展了便携式野外净水器的设计和制作。
解答题
试题详情
某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
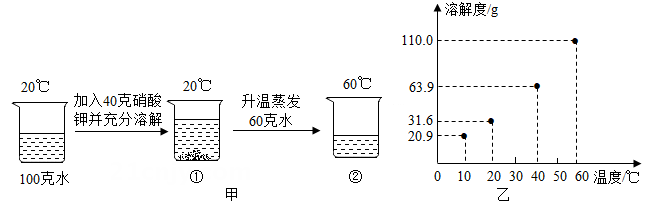
试题详情
思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小科建构了“混合物提纯”的思维模型:
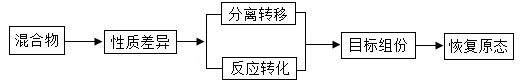
试题详情
一水硫酸四氨合铜的化学式为[Cu(NH3)4]SO4·H2O,是一种高效、安全的杀菌剂。它在以氧化铜为主要原料合成该物质,他设计的合成路线如图乙所示:


试题详情
某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
试题详情
下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
温度/℃ | 0 | 10 | 20 | 30 | 40 |
溶解度/克 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
试题详情
为研究“不同物质在敞口容器久置后的质量变化”,某科学兴趣小组将10.00克下列物质分别盛放于相同的烧杯中,将它们敞口放置在恒温实验室。一段时间后,测得烧杯中物质减小的质量情况见下表。
| 放置时间(小时) | 烧杯中物质减小的质量(克) | |||
| 水 | 饱和氯化钠溶液 | 饱和硝酸钾溶液 | 7.3%的稀盐酸 | |
| 24 | 1.85 | 0.61 | 0.72 | 1.35 |
| 48 | 3.70 | ? | 1.44 | 2.80 |
请回答: