单选题
- A、 锅炉水垢中含有的CaSO4 , 可先用Na2CO3溶液处理,后用酸除去
- B、 泡沫灭火剂利用了硫酸铝溶液与碳酸氢钠溶液混合后能发生剧烈双水解反应
- C、 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释
- D、 明矾净水与自来水的杀菌消毒原理相同
- A、 常温常压下,1 mol
溶于1.0 L
中,溶液中
的个数之和为2
- B、 标准状况下,11.2 L
与11.2 L HF均含有5
个质子
- C、 56.0 g Fe与1.0 mol
反应,转移电子数为2
- D、 46.0 g
完全燃烧,有5
个C-H键断裂
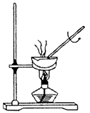
- A、 用向上排空气法收集氨气
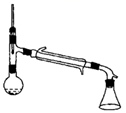
- B、 用焰色反应鉴别NaCl和KNO3
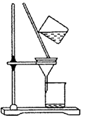
- C、 用饱和食盐水除去Cl2中混有的HCl
- D、 用Cl2除去FeCl3溶液中混有的FeCl2
- A、 氢氧化镁溶于稀醋酸:
- B、 将ClO2气体通入H2O2、NaOH的混合溶液中制取NaClO2溶液:
- C、 苯酚钠溶液中通入少量CO2:
- D、 用氢氧化钠溶液吸收二氧化氮:
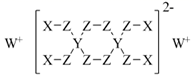
- A、 X、Z可形成具有强氧化性的高效消毒剂
- B、 Y的最高价氧化物对应的水化物中,除了氢原子外所有原子满足8电子稳定结构
- C、 由Z和W形成的化合物中可以存在共价键
- D、 X、Y、Z的原子半径从大到小为: Y > Z >X
|
| 实验 | 现象 | 结论 |
| A | 将过量铁粉加入硝酸中充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色. | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0 mol·L-1的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色 固体出现 | 金属Fe比Cu活泼 |
| C | 向Na2SiO3溶液中通入足量的CO2 | 产生白色胶状物质 | 非金属性:C>Si . |
| D | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液一定为钠盐溶液 |
- A、 A
- B、 B
- C、 C
- D、 D
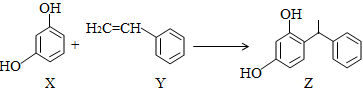
下列叙述正确的是( )。
- A、 X、Y和Z均能使溴水褪色,且原理相同
- B、 X和Z均能与Na2CO3溶液反应放出CO2
- C、 X、Y和Z分子中的所有原子可能共平面
- D、 X苯环上一氯代物有3种,Y苯环上的二氯代物有6种
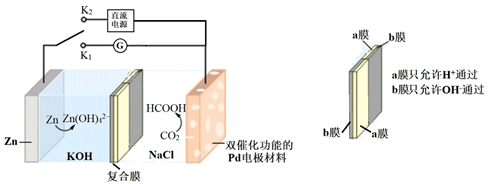
下列说法错误的是( )
- A、 闭合K1时,Zn表面的电极反应式为Zn + 4OH− - 2e− = Zn(OH)
- B、 闭合K1时,反应一段时间后,NaCl溶液的pH减小
- C、 闭合K2时,Pd电极与直流电源正极相连
- D、 闭合K2时,H+通过a膜向Pd电极方向移动

已知废渣中含有Fe(OH)3。下列说法错误的是( )
- A、 “酸溶”时的不溶物成分主要为硅酸和硫酸钡
- B、 为了加快反应速率,“酸溶”时,可采取搅拌、高温等措施
- C、 “中和Ⅰ”加入的X可选用BaCO3
- D、 废渣经过加工可用来生产油漆或涂料
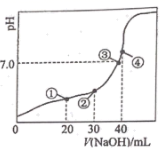
- A、 滴定过程中,当 pH=4 时,存在:c(H+)+c(Na+ )=c(OH- )+c(
)+c(
)
- B、 点①、③、④所示溶液中,点③所示溶液水的电离程度最大
- C、 点③所示溶液:3c(
)+2c(
)+c(H2C2O4)=0.1 mol•L-1
- D、 滴定过程中可能出现:c(Na+)>c(
)=c(
)>c(OH-)>c(H+)
| 容器 | 容积/L | 起始物质的量/mol | ||
| | | | ||
| Ⅰ | | 0.1 | 0 | 0 |
| Ⅱ | 1.0 | 0.1 | 0 | 0 |
| Ⅲ | | 0.1 | 0 | 0 |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |
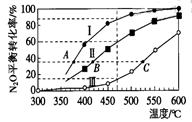
- A、 该反应的正反应放热
- B、 相同温度下反应相同时间,平均反应速率:
- C、 图中A,B,C三点处容器内总压强:
- D、 容器Ⅳ在470℃进行反应时,起始速率:
<
综合题
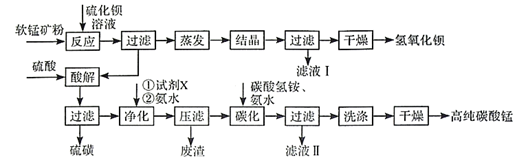
已知:MnO2是一种两性氧化物;25℃时相关物质的Ksp见下表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | | | | |
回答下列问题
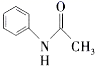 )在工业上可作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过本胺(
)在工业上可作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等,可通过本胺( 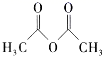 )反应制得。
)反应制得。 已知:纯乙酰苯胺是白色片状晶体,相对分子质量为135,熔点为114℃,易溶于有机溶剂。在水中的溶解度如下。
| 温度 | 20 | 25 | 50 | 80 | 100 |
| 溶解度/(g/100g水) | 0.46 | 0.56 | 0.84 | 3.45 | 5.5 |
实验室制备乙酰苯胺的步骤如下(部分装置省略):
Ⅰ.粗乙酰苯胺的制备。将7mL(0.075mol)乙酸酐放入三口烧瓶c中,在恒压滴液漏斗a中放入5mL(0.055mol)新制得的苯胺。将苯胺在室温下逐滴滴加到三口烧瓶中。苯胺滴加完毕,在石棉网上用小火加热回流30min,使之充分反应。待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有100mL冷水的烧杯中,乙酰苯胺晶体析出。充分冷却至室温后,减压过滤,用( )洗涤晶体2~3次。用滤液冲洗烧杯上残留的晶体,再次过滤,两次过滤得到的固体合并在一起。

Ⅱ.乙酰苯胺的提纯。将上述制得的粗乙酰苯胺固体移入250mL烧杯中,加入100mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,趁热过滤。待滤液冷却至室温,有晶体析出,( ),称量产品为3.28g。
回答下列问题:
①CH4(g)+H2O(g)⇌CO(g)+3H2 (g) △H1= 206kJ•mol-1
②CO(g)+H2O(g)⇌CO2(g)+H2(g) △H2= - 4 1 kJ•mol-1
近期报道,用二氧化碳作为氧化剂和甲烷重整制氢的新反应路线如下,可生成适宜 H2/ CO 的合成气。
③CH4 (g)+CO2 (g)⇌2CO(g)+2H2(g) △H3
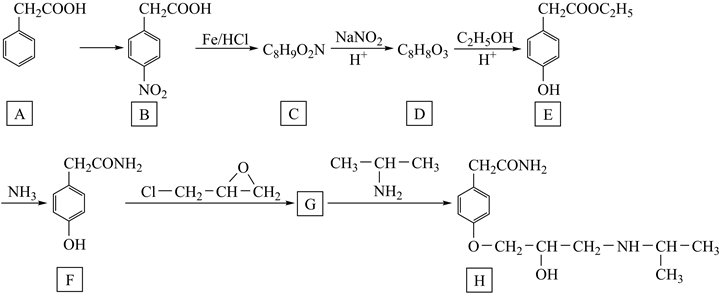 回答下列问题:
回答下列问题: