选择题(共20小题,满分40分,每小题2分)
试题详情
利用浓差电池制备高铁电池的重要材料Na2FeO4 , 反应原理如图所示。下列说法错误的是( )
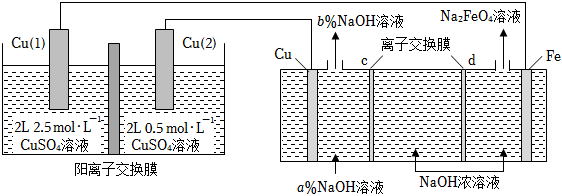
- A、 a<b
- B、 c为阳离子交换膜,当Cu电极产生1mol气体时,有2molNa+通过阳离子交换膜
- C、 浓差电池放电过程中,Cu(Ⅰ)电极上的电极反应为Cu﹣2e﹣=Cu2+
- D、 Fe电极的电极反应为:Fe+8OH﹣﹣6e﹣═FeO42﹣+4H2O
试题详情
硫酸甲酯(CH3OSO3H)是制造染料的甲基化试剂,在有H2O存在的条件下,CH3OH和SO3的反应历程如图所示(分子间的作用力用“…”表示)。下列说法错误的是( )
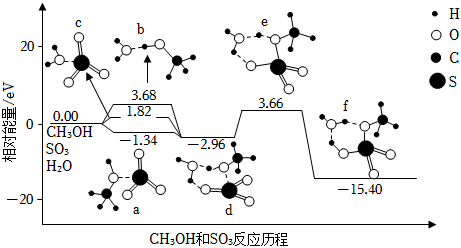
- A、 CH3OH与SO3反应的△H<0
- B、 a、b、c三种中间产物中,a最稳定
- C、 该反应最高能垒(活化能)为19.06eV
- D、 由d转化为f过程中,有硫氧键的断裂和生成
试题详情
下列说法不正确的是( )
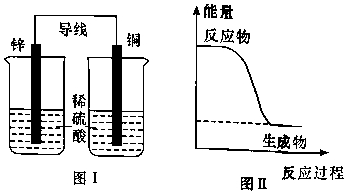
- A、 图Ⅰ所示装置不能形成原电池
- B、 铅蓄电池为二次电池,充电时,铅电极接外接电源的正极
- C、 燃料电池是一种将燃料和氧化剂的化学能直接转化为电能的装置
- D、 反应NH3(g)+HCl(g)═NH4Cl(s)的能量变化如图Ⅱ所示,则该反应在低温下能自发进行
试题详情
某化学反应X+Y→Z分两步进行:①X→M;②M+Y→Z。其能量变化如图所示。下列说法正确的是( )
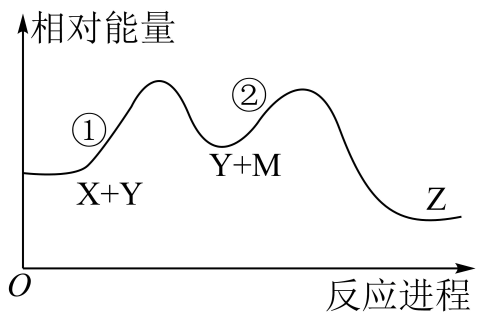
- A、 M是总反应的催化剂
- B、 总反应是理想的绿色化学反应
- C、 反应①②和总反应都是放热反应
- D、 反应物(X和Y)的总能量低于产物(Z)的总能量
试题详情
绿色电源“二甲醚﹣氧气燃料电池”的工作原理如图,所示下列说法正确的是( )
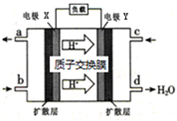
- A、 氧气应从c处通入,电极Y上发生的反应为O2+4e﹣+2H2O═4OH﹣
- B、 电池在放电过程中,电极X周围溶液的pH增大
- C、 二甲醚应从b处加入,电极X上发生的反应为(CH3)2O﹣12e﹣+3H2O=2CO2+12H+
- D、 当该电池向外电路提供2mol电子时消耗O2约为22.4L
试题详情
国家能源局发布2021年前三季度全国光伏发电建设运行情况,前三季度新增并网容量2555.6万千瓦,下列如图为光伏并网发电装置,甲基氢氧化铵[(CH3)4NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH3)4NCl]为原料,采用电渗析法合成[(CH3)4NOH],其工作原理如图所示,下列叙述中不正确的是( )

- A、 光伏并网发电装置是利用原电池原理,图中N型半导体为负极,P型半导体为正极
- B、 a极电极反应式:2(CH3)4N++2H2O+2e﹣=2(CH3)4NOH+H2↑
- C、 制备18.2g(CH3)4NOH,两极共产生4.48L气体(标准状况)
- D、 c、e为阳离子交换膜,d均为阴离子交换膜
试题详情
下列说法正确的是( )
- A、 增大反应物浓度可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
- B、 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
- C、 升高温度能使化学反应速率增大的主要原因是增加了反应物分子中活化分子的百分数
- D、 催化剂能增大单位体积内活化分子的百分数,使平衡转化率增大
试题详情
化学与社会、生活密切相关,下列说法正确的是( )
- A、 氢氧化铝、碳酸钠常用作胃酸中和剂
- B、 水泥和沙子都属于建筑材料中的硅酸盐产品
- C、 胆矾可用于杀菌消毒,也可作食品防腐剂
- D、 治理雾霾的有效方法是从源头上控制形成雾霾的污染物
试题详情
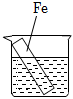
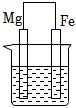
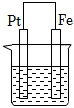
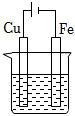
某小组为研究电化学原理,设计如图装置.下列叙述正确的是( )

- A、 a和b用导线连接时,铁片上会有金属铜析出
- B、 a和b用导线连接时,铜片上发生的反应为:Cu2+﹣2e﹣=Cu
- C、 无论a和b是否连接,铁片均会溶解
- D、 无论a和b是否连接,铁片上发生的反应都是:Fe﹣3e﹣=Fe3+
试题详情
苯的亲电取代反应分两步进行,可表示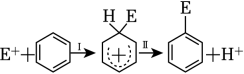 , 苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )
, 苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )
 , 苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )
, 苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )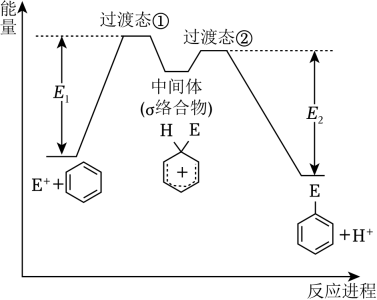
- A、 反应过程中,环上碳原子的杂化类型发生了变化
- B、 反应速率:Ⅰ<Ⅱ
- C、 平均能量:中间体>反应物
- D、 E1与E2的差值为总反应的焓变
试题详情
若要在铁片上镀银,下列叙述中错误的是( )
①将铁片接在电源的正极上
②将银片接在电源的正极上
③在铁片上发生的反应是:Ag++e﹣═Ag
④在银片上发生的反应是:4OH﹣﹣4e﹣═O2↑+2H2O
⑤需用硫酸铁溶液为电镀液
⑥需用硝酸银溶液为电镀液
- A、 ①③⑥
- B、 ②③⑥
- C、 ①④⑤
- D、 ②③④⑥
试题详情
下列说法错误的是( )
- A、 需要加热才能发生的反应一定是吸热反应
- B、 在热化学方程式中无论反应物还是生成物均必须标明聚集状态
- C、 焓变小于0而熵变大于0的反应肯定是自发的
- D、 轮船水线以下的船体上嵌入一定量的锌块可减缓海水对轮船的腐蚀
试题详情
如图,甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是( )

- A、 甲池通入CH3OH的电极反应式为CH3OH+6e﹣+2H2O=CO32﹣+8H+
- B、 甲池中消耗224mL(标准状况)O2 , 此时丙池中理论上产生1.16g固体
- C、 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
- D、 若将乙池电解质溶液换成AgNO3溶液,则可以实现在石墨棒上镀银
试题详情
铅酸电池是一种可充电电池,其放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O。如图所示,利用铅酸电池电解Na2SO4溶液(a、b均为石墨电极),可以制得H2、O2、较浓的H2SO4和NaOH溶液。下列说法正确的是( )

- A、 铝酸电池放电一段时间后,正、负极的质量均增加
- B、 N和M溶液分别为稀H2SO4和稀NaOH溶液
- C、 a电极的电极反应式为2H2O﹣4e﹣═O2↑+4H+
- D、 当电路中有1mol电子通过时,b电极收集到的O2体积为5.6L
试题详情
可逆反应N2+3H2⇌2NH3(各物质均为气体)的正、逆反应速率可用单位时间内各反应物或生成物浓度的变化来表示.下列各关系中能说明该反应已达到平衡状态的是( )
- A、 3v正(N2)=v正(H2)
- B、 v正(N2)=v逆(NH3)
- C、 2 v正(H2)=3 v逆(NH3)
- D、 2v逆(NH3)=3 v正(H2)
试题详情
下列说法中正确的是( )
- A、 钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO3而排出
- B、 珊瑚虫从周围海水中获取Ca2+和HCO3﹣ , 经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚
- C、 水中的Mg(HCO3)2、Ca(HCO3)2 , 受热易分解生成难溶性的MgCO3、CaCO3 , 故水垢的主要成分是MgCO3、CaCO3
- D、 使用含氟牙膏预防龋齿利用了盐类水解的原理
试题详情
乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示.下列说法不正确的是( )
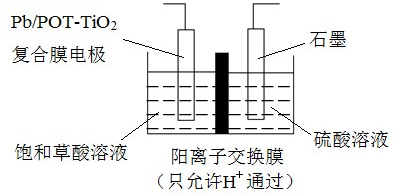
- A、 电解时石墨电极应与直流电源的正极相连
- B、 阴极反应式为:HOOCCOOH+2H++2e﹣═OHCCOOH+H2O
- C、 电解时石墨电极上有O2放出
- D、 电解一段时间后,硫酸溶液的pH不变化
试题详情
熔融状态下,Na和FeCl2能组成可充电电池(装置如图所示),反应原理为:2Na+FeCl2 Fe+2NaCl下列关于该电池的说法正确的是( )
Fe+2NaCl下列关于该电池的说法正确的是( )
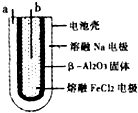
- A、 放电时,a为正极,b为负极
- B、 放电时,负极反应为:Fe2++2e﹣=Fe
- C、 充电时,a接外电源正极
- D、 充电时,b极处发生氧化反应
解答题(共1小题,满分3分,每小题3分)
试题详情
电池种类丰富,发展飞速,应用广泛,为我们的生产和生活带来了非常大的便利。
解答题(共2小题,满分6分,每小题3分)
试题详情
环己酮(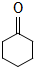 )是重要的化工原料。实验室氧化环己醇制备环己酮的流程如图:
)是重要的化工原料。实验室氧化环己醇制备环己酮的流程如图:
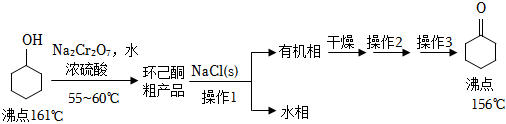
回答下列问题:
试题详情
氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
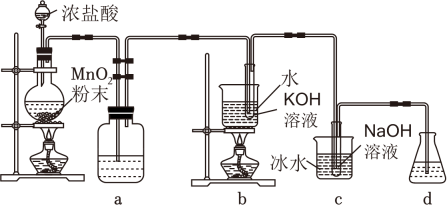
请回答下列问题:
推断题(共1小题,满分3分,每小题3分)
试题详情
某兴趣小组对无机盐X (仅含三种短周期元素)开展探究实验。
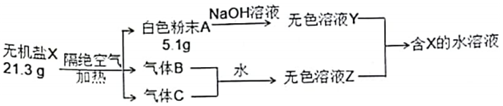
其中:A、B、C均为纯净物,白色粉末A难溶于水,B为红棕色气体。生成的B和C气体恰好与水完全反应(无气体剩余)生成溶液Z。请回答: