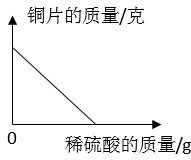
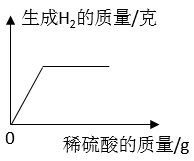
单选题
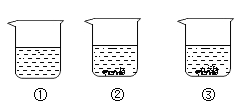
- A、 ①中所得溶液一定是不饱和溶液
- B、 ②③中所得溶液溶质的质量分数相等
- C、 若②中溶液升温到30℃,溶液的质量一定不变
- D、 若③中溶液恒温蒸发,溶质的质量分数一定变大

- A、 由实验可判断出铁、铜、锌的活动性顺序
- B、 两支试管混合后,固体总质量一定增加
- C、 滤渣中一定有Cu,一定没有Fe和Zn
- D、 滤液中的溶质一定有FeCl2、ZnCl2和CuCl2
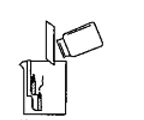
- A、 实验室制取二氧化碳的药品为块状大理石和稀硫酸
- B、 实验室可采用向上排空气法收集二氧化碳
- C、 图示实验可说明二氧化碳密度比空气大
- D、 图示实验可说明二氧化碳不支持蜡烛的燃烧
| 选项 | 实验目的 | 操作 |
| A | 用氯酸钾和二氧化锰制取氧气后,回收其中的二氧化锰 | 将反应得到的混合物溶解后直接加热蒸发 |
| B | 用向上排空气法收集氧气时,检验氧气是否收集满 | 用带火星的木条伸人到集气瓶中,观察木条是否复燃 |
| C | 鉴别盐酸和硫酸 | 取样后滴加氯化钡溶液,观察是否变浑浊 |
| D | 比较铜和银的化学活动性顺序 | 将两种金属与等质量且同浓度的盐酸反应,观察产生气泡的快慢 |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 2.5%
- B、 4.5%
- C、 5%
- D、 7%
填空题

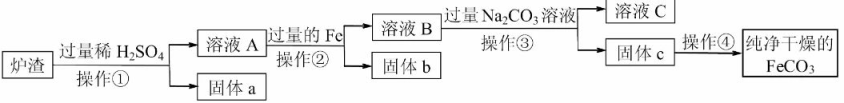
【已知:Fe+Fe2(SO4)3=3FeSO4;SiO2不溶于水,也不与稀硫酸反应】
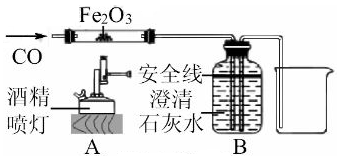

实验探究题

猜想一:Ca(OH)2溶液与CO2不反应,是CO2溶于水导致瓶内气压变小而变瘪。
猜想二:Ca(OH)2溶液与CO2反应,生成了可溶性物质。
| 实验 | 步骤与操作 | 出实验现象与结果 光 | 结论 |
| 一 | 1.取2个相同的软塑料瓶,分别集满CO2气体,编号为A、B。 | 两瓶内气体无色透明,瓶子形状正常 | Ca(OH)2溶液与CO2发生了化学反应 |
| 分别向A、B两瓶中加入等量的饱和Ca(OH)2溶液和 ? , 立即拧紧瓶盖并振荡。 | 两瓶内液体未出现浑浊,两瓶均变瘪,A瓶变瘪程度更大。 | ||
| 二 | 测出反应前Ca(OH)2溶液的pH。 | 大于7。 | |
| 测出反应后A瓶内液体的pH。 | 小于7。 |
甲同学:将镁带和铜粉分别在酒精灯的外焰上加热,观察现象。
乙同学:把铁制容器和铝制容器放在同一潮湿环境中,一段时间后观察容器表面的锈蚀情况。
……
实验后,同学们进行汇报和评价交流。

【实验步骤】
①取一根玻璃管,用橡皮塞将一端密封;
②将食品脱氧剂粉末迅速装入玻璃管,立即向管口注入一滴水将玻璃管密封,水滴的下端标为A。
弹动玻璃管使脱氧剂粉末分布均匀且紧密,脱氧剂的上端标为O,如图甲所示;
③水平滚动玻璃管,使食品脱氧剂粉末平铺在玻璃管中。静置至水滴不再移动时,水滴的右端标为B,如图乙所示;
④用刻度尺测量出AO段和AB段的长度,并计算出AB
与AO的比值,将数据记录在表格中;
⑤洗涤、干燥实验装置,重复上述实验。
| 实验次数 | AO/mm | AB/mm | AB / AO |
| 1 | 523.5 | 109.5 | 0.2092 |
| 2 | 525.5 | 110.0 | 0.2093 |
| 3 | 527.0 | 110.5 | 0.2097 |
【得出结论】 根据表格中的实验数据, 可知空气中氧气含量为。(用百分数表示)
【思考讨论】
①实验步骤③中,将食品脱氧剂粉末平铺在玻璃管中的目的是。
②实验步骤②中,如果玻璃管内的脱氧剂粉末分布不够紧密,会使实验结果偏大,其原因是。