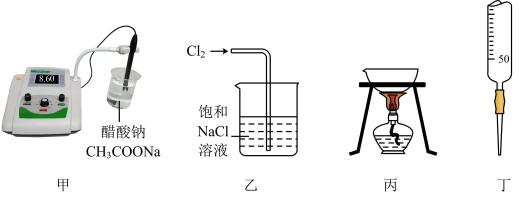
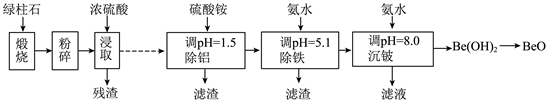
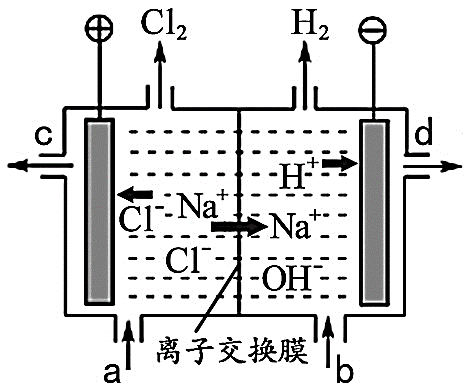
单项选择题(本题共14小题,每小题3分,共42分)
试题详情
华容县有很多风味独特的美食,其中火锅类菜品以酸辣香鲜出名。火锅底料的配料有食盐、白糖、陈醋、味精、辣椒、黄酒、生姜、油脂等。下列配料属于弱电解质的是( )
- A、 C2H5OH
- B、 CH3COOH
- C、 NaCl
- D、 白糖
试题详情
反应N2(g)+O2(g)=2NO(g)的能量变化如图所示。已知:断开1molN2(g)中化学键需吸收946kJ能量,断开1molO2(g)中化学键需吸收498kJ能量。下列说法正确的是( )
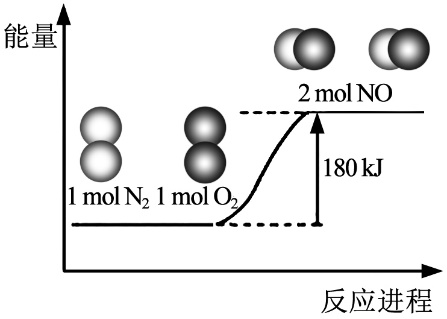
- A、 N2(g)+O2(g)=2NO(g) △H=-180kJ/mol
- B、 NO(g)=1/2N2(g)+1/2O2(g) △H=+90kJ/mol
- C、 断开1molNO(g)中化学键需要吸收632kJ能量
- D、 形成1molNO(g)中化学键可释放90kJ能量
试题详情
工业上苯乙烯的生产主要采用乙苯脱氢工艺:C6H5CH2CH3(g)C6H5CH=CH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是( )
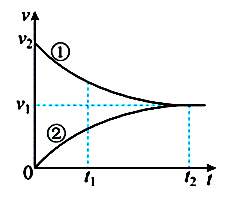
- A、 曲线①表示的是逆反应的v-t关系
- B、 t1时刻体系处于平衡状态
- C、 反应进行到t1时,Q>K(Q为浓度商)
- D、 当加入正催化剂存在时,ν1、ν2都增大
试题详情
测定浓硫酸试剂中H2SO4含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取20.00mL待测液,用0.1mol/L的NaOH溶液滴定。上述操作中,不需要用到的仪器为( )
- A、
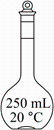
- B、
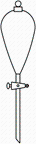
- C、
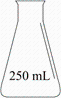
- D、

试题详情
向恒温恒容密闭容器中通入2molSO2和1molO2 , 反应2SO2(g)+O2(g) 2SO3(g)达到平衡后,再通入一定量O2 , 达到新平衡时,下列有关判断错误的是( )
2SO3(g)达到平衡后,再通入一定量O2 , 达到新平衡时,下列有关判断错误的是( )
- A、 SO3的平衡浓度增大
- B、 反应平衡常数增大
- C、 正向反应速率增大
- D、 SO2的转化总量增大
试题详情
下列溶液中,一定呈中性的是( )
- A、 由非电解质溶于水得到的溶液
- B、 c(H+)、c(OH-)均为5.0×10-7mol·L-1的溶液
- C、 等物质的量的强酸与强碱反应得到的溶液
- D、 将pH=9的烧碱溶液稀释100倍所得到的溶液
试题详情
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
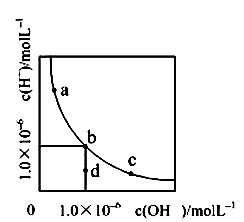
- A、 升高温度,可能引起有c向b的变化
- B、 该温度下,水的离子积常数为1.0×10‾13
- C、 该温度下,加入FeCl3可能引起由b向a的变化
- D、 该温度下,稀释溶液可能引起由c向d的变化
试题详情
设NA为阿伏加德罗常数值。关于常温下pH=2的H3PO4溶液,下列说法正确的是( )
- A、 每升溶液中的H+数目为0.02NA
- B、 c(H+)=c(
)+2c(
)+3c(
)+c(OH−)
- C、 加水稀释使电离度增大,溶液pH减小
- D、 加入NaH2PO4固体,溶液酸性增强
试题详情
短周期元素X、Y、Z、W的原子序数依次增大。W原子的最外层电子数是X与Z原子最外层电子数之和,W简单氢化物r溶于水完全电离。m、p是由这些元素组成的二元化合物,m可做制冷剂,无色气体p遇空气变为红棕色。下列说法正确的是( )
- A、 简单离子半径:W>Z>Y>X
- B、 Y原子的价电子轨道表示式为

- C、 r与m可形成离子化合物,其阳离子电子式为
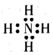
- D、 一定条件下,m能与Z的单质反应生成p
试题详情
将图1所示装置中的盐桥(琼脂—饱和 溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是( )
溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是( )
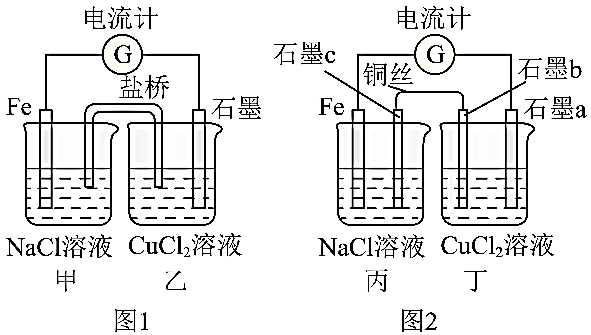
- A、 图1中,铁棒质量减少
, 则乙池
溶液的质量减少
- B、 图2丙池中石墨c电极附近
减小
- C、 图1中的石墨电极与图2中丁池石墨b电极的电极反应式相同
- D、 图2中电流方向为石墨c→铜丝→石墨b→石墨a→电流计