单选题

- A、 常温下,醋酸钠属于微溶物质
- B、 图中P点所表示的醋酸钠溶液是不饱和的
- C、 40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
- D、 将A点的饱和溶液降温至20℃,溶质质量分数增大
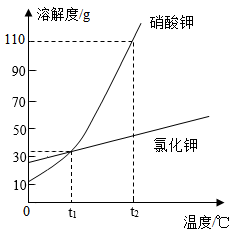
- A、 氯化钾的溶解度随温度的升高而增大
- B、 t1℃时,硝酸钾和氯化钾的溶解度相等
- C、 将t1℃时的硝酸钾饱和溶液升温至t2℃,溶质质量不变
- D、 t2℃时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:21

- A、 0℃时,NH4Cl的溶解度大于NaCl的溶解度
- B、 NH4Cl中含有少量NaCl,可用降温结晶的方法提纯NH4Cl
- C、 20℃时,NaHCO3饱和溶液的溶质质量分数一定大于NH4Cl不饱和溶液的溶质质量分数
- D、 20℃时,将9.6gNaHCO3加入到90.4g水中,可得到100g饱和溶液

- A、 a1℃时,甲、乙的溶解度相同
- B、 甲的溶解度受温度影响比乙小
- C、 当甲中混有少量乙时,可采用蒸发的方法提纯甲
- D、 a2℃时,在100g水中加入30g甲,形成饱和溶液
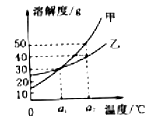
- A、 甲的溶解度一定大于乙的溶解度
- B、 升高温度可以将甲和乙的饱和溶液转化为不饱和溶液
- C、 α2℃时甲的饱和溶液中溶质和溶剂的质量比为1:3
- D、 α2℃时相同质量的甲和乙溶液,降温至α1℃时甲溶液析出的晶体一定比乙溶液多
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | 甲 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 |
乙 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
丙 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
- A、 固体甲的溶解度随温度的升高而增大
- B、 20℃时,丙溶液中溶质和溶剂质量比为31.6:100
- C、 分别将等质量的乙、丙饱和溶液由60℃降温到20℃,溶质质量大小:丙>乙
- D、 分别将等质量的甲、丙饱和溶液由60℃降温到20℃,溶剂质量大小:甲>丙
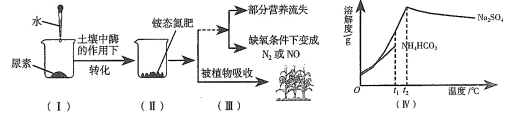
- A、 (Ⅰ)中氮元素可直接被植物吸收
- B、 (Ⅱ)生成的铵态氮肥一定含NH4Cl
- C、 (Ⅲ)暴雨会使铵态氮肥营养流失
- D、 (Ⅳ)降温结晶可使两种物质分离

- A、 碳酸钠的溶解度随温度升高而增大
- B、 将20℃的碳酸钠饱和溶液升温至30℃,溶质质量分数不变
- C、 30℃时,将25g碳酸钠加入50g水中,所得溶液质量为75g
- D、 40℃时,碳酸钠饱和溶液的溶质质量分数为50%

- A、 (Ⅰ)中氮元素可直接被植物吸收
- B、 (Ⅱ)生成的铵态氮肥一定含NH4Cl
- C、 (Ⅲ)碱性土壤使铵态氮肥营养流失
- D、 (Ⅳ)降温结晶可使两种物质分离

- A、 烧杯中剩余固体的质量为13g
- B、 再加入100g水,充分溶解后烧杯中仍有固体剩余
- C、 升温至40℃,溶液的质量分数约为31.5%
- D、 升温至60℃,溶液变为不饱和溶液
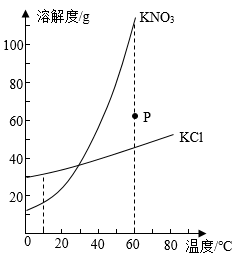
- A、 10℃时,KNO3的溶解度比KCl大
- B、 KCl的溶解度受温度影响的程度比KNO3大
- C、 60℃时,P点表示的KNO3溶液还能继续溶解KNO3固体
- D、 将60℃的KCl饱和溶液降温至10℃,溶液中溶质质量分数不变

- A、 甲烧杯中的溶质为KNO3
- B、 将温度升高到t2℃时,乙烧杯中仍然有固体剩余
- C、 若KNO3中混有少量KCl,可采用蒸发结晶的方法提纯KNO3
- D、 若取t3℃时KNO3和KCl的饱和溶液各100g,降温至t2℃时,析出晶体较多的是KNO3
温度/℃ | 0 | 10 | 20 | 30 |
NH4HCO3溶解度(g/100g水) | 11.9 | 15.8 | 21.0 | 27.0 |
- A、 用NH4HCO3晶体配制浓溶液时,可加热煮沸以加快溶解
- B、 NH4HCO3是铵态复合肥料,与其它肥料都可以混合使用
- C、 20℃时,50.0g蒸馏水就能使11.0g NH4HCO3晶体完全溶解
- D、 127.0g NH4HCO3饱和溶液,由30℃降至20℃可析出6.0g晶体
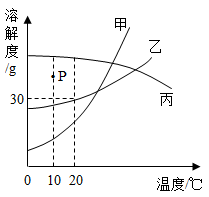
- A、 图中P点表示10℃时丙的饱和溶液
- B、 10℃时,甲、乙、丙三种物质的溶解度,甲的溶解度最大
- C、 20℃时,甲、乙、丙饱和溶液降温至10℃,甲溶液中析出固体最多
- D、 20℃时,向130g乙的饱和溶液中加入20g水,所得溶液的溶质质量分数变为20%

结合硝酸钾在不同温度下的溶解度,判断下列说法错误的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
KNO3溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
- A、 ①③中的溶液均为不饱和溶液
- B、 ②③中溶液的质量:③>②
- C、 ②③④中溶液的溶质质量分数:③>②>④
- D、 ④中析出晶体的质量是0.9g

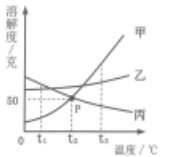
- A、 高于t1℃时甲溶液溶质质量分数一定更大
- B、 降温是将a处的甲溶液变饱和的唯一方法
- C、 t1℃时50g乙投入水中一定能完全溶解
- D、 t2℃时相同质量的甲、乙饱和溶液,乙溶液中溶剂质量更大

温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
- A、 若a是NaCl,则③中的溶液是不饱和溶液
- B、 若a是NaCl,则④中溶质的质量分数约为27.2%
- C、 若a是KNO3 , 则③到④溶液由不饱和转化为饱和
- D、 实验证明溶液是否饱和与温度、溶质的量和溶剂种类有关
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |

- A、 曲线甲代表KCl的溶解度曲线
- B、 40℃时KNO3饱和溶液中KNO3的质量分数为63.9%
- C、 t1的值在20~30之间
- D、 将t1℃时甲和乙的饱和溶液升温至t2℃时,溶液中溶质的质量分数:甲>乙
图像 | 描述 |
| 向盛有HCl和BaCl2的混合溶液中,逐滴滴入一定溶质质量分数的NaOH溶液至过量 |
| 1g硫和1g氧气在密闭容器中充分反应 |
| NaOH和NaCl固体分别溶于室温下足量的水中 |
| 向氢氧化钙的饱和溶液中加入一定量的氧化钙固体 |
- A、 1个
- B、 2个
- C、 3个
- D、 4个
多选题


| KNO3和KCl在不同温度时的溶解度表 | |||||||||
| 温度/℃ | 0 | T1 | 20 | T2 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 25.0 | 31.6 | 35.1 | 63.9 | 110 | 169 | 246 |
| KCl | 27.6 | 31.8 | 34.0 | 35.1 | 40.0 | 45.5 | 51.1 | 56.7 | |
下列说法正确的是( )
- A、 乙烧杯中加入的固体一定是KNO3
- B、 图1中溶液可能是该溶质的饱和溶液,图2中上层清液一定是该溶质的饱和溶液
- C、 若从T1℃重新升高到T2℃,甲、乙两溶液中的溶质质量分数一定不相等
- D、 a的取值范围为31.8<a≤35.1
选择填充题
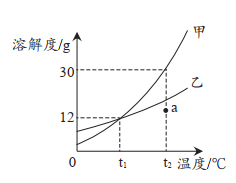
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,100g甲、乙两种物质的溶液中所含溶质的质量相等
C.将a点的乙溶液转化为饱和溶液,溶质质量分数不一定改变
D.t2℃时,在50g水中加入20g甲物质所得溶液的质量为g
填空题
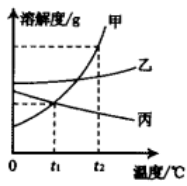
t1℃时甲、乙、丙溶解度最大的是,将该温度时三种物质的饱和溶液升温到t2℃(不考虑溶剂蒸发),有固体析出的是,此时所得溶液的溶质质量分数由大到小的顺序是。
综合题






温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | |





温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
NaCl的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
NH4Cl的溶解度/g | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |


温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |

溶解度S | 溶解性 |
S≥10g | 易溶 |
10g>S≥lg | 可溶 |
1g>S≥0.0lg | 微溶 |
S<0.01g | 难溶 |

温度/C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |


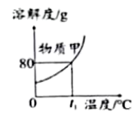 t1℃时,50g甲能完全溶于50g水
t1℃时,50g甲能完全溶于50g水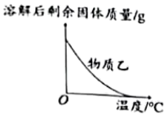 乙的溶解度随温度升高而降低
乙的溶解度随温度升高而降低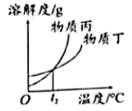 t2℃时,丙和丁的溶解度相同
t2℃时,丙和丁的溶解度相同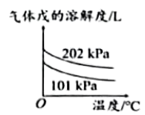 加压或升温能增加戊的溶解度
加压或升温能增加戊的溶解度




