选择题
试题详情
室温下,甲同学配制5%的 溶液100g,乙同学配制
溶液100g,乙同学配制 的
的 溶液100mL(
溶液100mL( 的溶解度为
的溶解度为 水),下列说法正确的是
水),下列说法正确的是
- A、 所需溶质的质量相同
- B、 所需仪器均包括100mL容量瓶
- C、 所配溶液均为不饱和溶液
- D、 所配溶液质量相同
试题详情
下列关于容量瓶使用方法的叙述中,正确的是( )
①使用容量瓶前检查是否漏水;
②在容量瓶中溶解固体溶质;
③溶液需冷却至室温方可注入容量瓶;
④尽可能将溶质全部转移到容量瓶中;
⑤加水定容时,不小心超过刻度线,用胶头滴管吸出多余液体
- A、 ①②③
- B、 ①③④
- C、 ③④⑤
- D、 ①④⑤
试题详情
下列操作可能使所配Na2CO3溶液浓度偏大的是( )
- A、 烧杯和玻璃棒未洗涤
- B、 称量前Na2CO3·10H2O固体已失去部分结晶水
- C、 加水时超过刻度线,用胶头滴管吸出多余的液体
- D、 上下颠倒摇匀后溶液液面低于刻度线,补充加水至刻度线
试题详情
实验室需要460mL0.20mol∙L-1Na2CO3溶液,某同学配制过程如图所示。
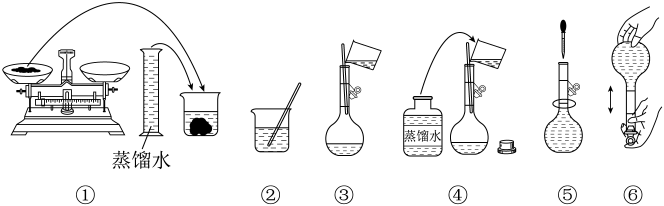
下列关于该实验的叙述错误的是
- A、 将药品放在称量纸上称取10.6gNa2CO3固体
- B、 Na2CO3固体在烧杯中完全溶解后,恢复至室温转移到容量瓶中定容
- C、 ⑤中定容时俯视刻度线会导致溶液浓度偏低
- D、 容量瓶不宜长期贮存配制好的溶液
试题详情
用18.4mol·L-1浓硫酸配制90mL 3mol·L-1的稀硫酸,下列说法错误的是
- A、 应选用100mL容量瓶
- B、 可选用量筒量取浓硫酸
- C、 量取的浓硫酸直接倒入容量瓶中
- D、 定容时应选用胶头滴管
试题详情
实验室欲配制100mL1.00mol/LNaCl溶液。下列操作及分析正确的是
- A、 用托盘天平称量物体时将氯化钠置于右盘的滤纸上
- B、 将称好的NaCl固体放入容量瓶中溶解
- C、 定容时俯视,所得溶液浓度偏高
- D、 摇匀时发现漏液,损失一部分溶液,再加水定容至刻度线
试题详情
有人提出溶液的浓度可用“质量摩尔浓度”(即一定质量的溶液中所含溶质的物质的量)表示。下列说法正确的是
- A、 配制一定质量摩尔浓度的溶液时,必须用到容量瓶
- B、 将溶液的质量摩尔浓度换算为其质量分数时,必须已知该溶液的密度
- C、 对于一种稀溶液(密度按
计),其质量摩尔浓度(
)与物质的量浓度(
)在数值上相等
- D、 分别取质量摩尔浓度相等的盐酸和NaOH溶液,等体积混合后一定恰好发生反应
多选题
试题详情
用绿矾(  )体配制一定物质的量浓度的
)体配制一定物质的量浓度的  溶液,下列操作正确的是( )
溶液,下列操作正确的是( )
试题详情
用胆矾配制0.1mol/L的硫酸铜溶液。下述方法中,最合理的是( )
试题详情
图中是某硫酸试剂瓶标签上的部分内容。用该硫酸试剂配制50.0 mL 4.6 mol·L-1的稀硫酸,下列说法错误的是( )
| 硫酸化学纯(CP) (500 mL) 化学式:H2SO4 相对分子质量:98 质量分数:98% 密度:1.84 g/mL |
试题详情
实验室需要配置100 mL 1.0×10-2 mol·L-1的CuSO4溶液,下列玻璃仪器中,一定要用到的有( )
试题详情
配制100mL1mol/L的氢氧化钠溶液,下列操作错误的是( )
试题详情
配制0.1mol•L﹣1NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是( )
试题详情
用容量瓶配制一定物质的量浓度的溶液,下列操作会使配制的NaOH溶液浓度偏低的是( )
非选择题
试题详情
水体的化学需氧量(COD)能反映水体受还原性物质污染的程度。某小组用高锰酸钾法测定学校周边河水的COD值。请回答下列问题:
I.配制200mL2.00×10-3mol•L-1的KMnO4溶液
试题详情
用10mol/L的浓盐酸配制成1mol/L的稀盐酸220mL。试回答下列问题:
试题详情
下面是用18mol/L的浓H2SO4稀释配制成500mL1mol/L的稀H2SO4的操作,请按要求填空:
试题详情
共和国勋章获得者钟南山院士强调,要注意疫情防控常态化,坚持做好日常消毒工作。含氯消毒剂在卫生防疫方面起着重要的作用。常见的含氯消毒剂有漂白粉、84消毒液等。
试题详情
在某次实验中,要用 420mL 0.52 mol·L-1的NaOH 溶液,回答下列问题:
试题详情
某兴趣小组配制氢氧化钡溶液
试题详情
实验室需要配制
 溶液
溶液 。
。
按下列操作步骤填上适当的文字,以使整个操作完整。
试题详情
小组同学用FeSO4•7H2O晶体和蒸馏水配制100mL0.5mol•L-1FeSO4溶液(pH为3.3),再进行性质探究实验。
试题详情
实验室用 固体配制100
固体配制100 1.00
1.00
 溶液,回答下列问题。
溶液,回答下列问题。
试题详情
根据所学知识回答问题:
试题详情
某小组配制100mL 1.0mol/L  溶液并进行实验。
溶液并进行实验。
试题详情
实验室需用500 mL 0.1 mol/L NaOH溶液,现用NaOH固体配制该溶液。请回答下列问题:
试题详情
实验小组同学需要配制 溶液。方法如下:
溶液。方法如下:
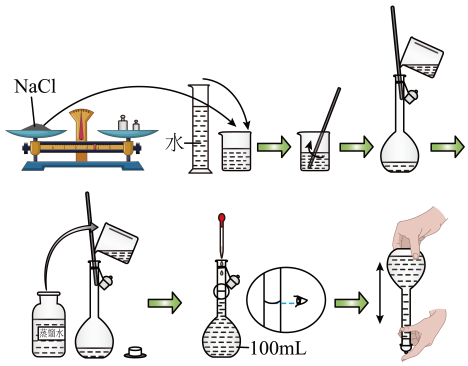
试题详情
实验室需要配制0.50 NaCl溶液480mL。按下列操作步骤填写适当的文字或数据,以使整个操作完整。
NaCl溶液480mL。按下列操作步骤填写适当的文字或数据,以使整个操作完整。
a.选择仪器。
完成本实验所必须用到的仪器有托盘天平(带砝码,最小砝码为5g)、药匙、烧杯、、玻璃棒、胶头滴管以及等质量的两片滤纸。
b.计算。
配制该溶液需取NaCl晶体g。
c.称量。将药品倒入烧杯中。
d.溶解、冷却。
该步实验中需要使用玻璃棒,其目的是。
e.转移、洗涤。
在转移时应使用玻璃棒引流,需要洗涤烧杯和玻璃棒2~3次,目的是。
f.振荡。轻轻摇动容量瓶,使溶液混合均匀。
g.定容。
将蒸馏水注入容量瓶至液面接近刻度线处,改用滴加,使溶液凹液面与刻度线相切
h.摇匀、装瓶
i.实验过程中的以下操作会导致最终所配溶液的浓度 (填“偏高”“偏低”或“无影响”):
实验操作 | 最终所配溶液的浓度 |
向容量瓶中移液时少量溅出 | |
定容时俯视刻度线 | |
定容摇匀后液面下隆再加水 | |
未等溶液冷却就定容 |
试题详情
用 固体配制100mL1.00mol/L
固体配制100mL1.00mol/L 溶液。
溶液。
试题详情
高锰酸钾溶液常用于物质的定性检验与定量分析。


