单选题
- A、
 用方案甲探究同种物质在不同溶剂中的溶解性
用方案甲探究同种物质在不同溶剂中的溶解性 - B、
 用方案乙探究空气是铁生锈的必要条件
用方案乙探究空气是铁生锈的必要条件 - C、
 用方案丙探究不同催化剂对H2O2分解速率的影响
用方案丙探究不同催化剂对H2O2分解速率的影响 - D、
 用方案丁探究合金及其成分金属的熔点高低
用方案丁探究合金及其成分金属的熔点高低
| 选项 | 实验 | 现象 | 结论 |
| A | 检验氢气的纯度
| 点燃氢气时发出尖锐爆鸣声 | 氢气较纯 |
| B | 称量盐酸和碳酸钠粉末反应前后的质量
| 反应前后称量结果不同 | 参加该反应的反应物质量总和不等于生成物质量总和 |
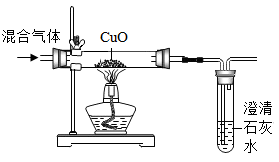
| C | 检验某混合气体的成分 | 黑色粉末变红,澄清石灰水变浑浊 | 混合气体中可能含有CO |
| D | 在酒精灯火焰上方罩一个冷而干燥的烧杯
| 烧杯内壁有无色液滴产生 | 酒精中含有碳元素和氢元素 |
- A、 A
- B、 B
- C、 C
- D、 D
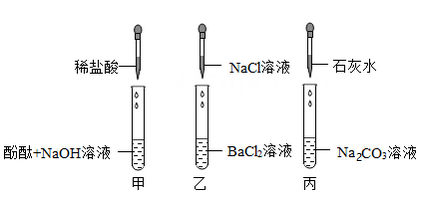
实验一:取少量样品于试管中,滴加1~2滴酚酞溶液,溶液显红色。
实验二:取少量样品于试管中,加入适量稀硫酸,有气泡放出。
实验三:取少量样品于试管中,加入足量的BaCl2溶液,有白色沉淀生成。过滤,向滤液中滴加1~2滴酚酞溶液,溶液显红色。
下列结论正确的是( )
- A、 实验一说明NaOH溶液没有变质
- B、 实验二说明NaOH溶液全部变质
- C、 实验三中生成的沉淀为Ba(OH)2
- D、 实验三说明NaOH溶液部分变质

- A、 若滤液1呈无色,则滤液2中可能会有Fe2+、Cu2+、Mg2+
- B、 若气体1为纯净物,则原固体X一定不含碳酸钙
- C、 若滤液2呈浅绿色,则滤渣1中一定含有铜、铁
- D、 若气体1为混合物,测滤渣1中一定含有碳酸钙、铜、铁


- A、 烧杯中只能盛放稀氢氧化钠溶液
- B、 图2不能证明反应是放热反应
- C、 60s时溶液中溶质只有氯化钠
- D、 实验证明氢氧化钠与盐酸能反应
多选题

综合题


实验探究题
【查阅资料】
鸡蛋膜有极其微小的孔隙。



【查阅资料】蛭石是一种耐高温的超级保温材料,难溶于水,不与硫酸铜溶液反应。

近年来,自热食品种类繁多。只需将撕去塑料膜的发热包放入凉水中,就能享用美食,很受年轻人的追捧。实验小组同学买来一份自热食品进行以下探究。
【资料】Ⅰ、发热包中物质的主要成分是生石灰、碳酸钠、铝粒。
Ⅱ、铝能和NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,偏铝酸钠溶于水。
小吴按照说明书将适量茶垢清洁剂放入有茶垢的杯子中,加入热水浸没茶垢,立即产生大量气泡,一段时间后冲洗茶杯,茶杯光亮如新。
【提出问题】兴趣小组在研究溶洞成因后提出:
在碳酸钠溶液中通入二氧化碳气体也会发生类似的反应吗?
推测反应方程式为:Na2CO3+H2O+CO2=2NaHCO3
【提出问题一】呼出的气体中有哪些物质与过氧化钠(Na2O2)发生反应,且生成物是什么?
【查阅资料】
①呼出的气体主要含有氮气、二氧化碳、水蒸气和氧气
②过氧化钠与氮气、氧气不反应
③过氧化钠为淡黄色固体粉末
①“问天”小组的猜想是:该溶液没有变质。
②“梦天”小组的猜想是:该溶液部分变质。
③“天和”小组的猜想是:该溶液全部变质。
三个小组的同学们根据各自猜想,分别进行如下实验:
【提出问题】氢氧化钠溶液是否变质及变质的程度?
【猜想与假设】①没有变质:②部分变质:③全部变质。
【实验与结论】
方案 | 实验操作 | 现象 | 结论 |
方案一 | 取该溶液2mL于试管中,滴入少量稀盐酸 | 无明显现象 | 没有变质 |
方案二 | 首先取该溶液2mL于试管中,滴入过量氯化钡溶液 | 溶液变浑浊 | 部分变质 |
静置,然后取上层清液放入试管中,滴入硫酸铜溶液 | 有蓝色沉淀产生 |
【查阅资料】
①干粉灭火器的主要成分为NaHCO3。
②NaHCO3受热分解生成Na2CO3、二氧化碳和水;Na2CO3受热不分解。
③NaHCO3溶液呈碱性,且不与BaCl2溶液发生反应。
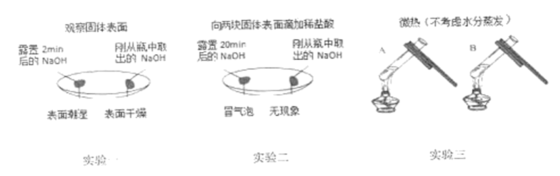
【猜想与假设】样品的成分可能是Ca(OH)2和CaCO3中的一种或两种。
【查阅资料】20℃时溶解度:Ca(OH)2—0.161g,CaCO3—0.005g。
【设计实验】学习小组设计如下实验进行探究。
编号 | 实验操作 | 实验现象 | 实验结论 |
① | 取样品于烧杯中,加入一定量的水溶解 | 温度无变化,烧杯底有白色固体 | 有CaCO3 |
② | 将①中液体过滤,取少量滤液于试管中,滴入1~2滴酚酞试液 | 溶液变红 | 有Ca(OH)2 |
③ | 有气泡产生 | 有CaCO3 |
【查阅资料】影响化学反应速率的因素有很多,如:使用催化剂、改变温度、改变反应物的浓度等。
【实验探究】小组的同学们按图组装,在室温下分别进行了四组实验,并用O2传感器测定实验过程中O2含量的变化情况,得到如下图所示曲线。
组别 | 试剂 |
第1组 | 2mL 5% H2O2 |
第2组 | 2mL 5% H2O2 + 3滴FeCl3溶液 |
第3组 | 2mL 5% H2O2 + 3滴CuSO4溶液 |
第4组 | 2mL 5% H2O2 +少量MnO2粉末 |


【实验结论】对比四条曲线,进行分析:
【查阅资料】
①Na是一种银白色金属,化学性质很活泼,常温下可与O2、H2O等物质发生反应,加热条件下与O2反应生成较复杂的氧化物。
②Na2O为白色固体,溶于水并与H2O反应生成NaOH,还能与CO2反应生成Na2CO3。
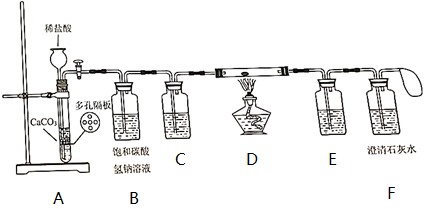
【实验过程】
③打开活塞,向长颈漏斗中加入适量盐酸,让产生的气体依次通过后面装置。
④待F中石灰水变浑浊,点燃酒精灯加热,金属钠熔化并开始燃烧,熄灭酒精灯,待钠燃烧完全且试管冷却后再关闭活塞,观察产物为白色固体。
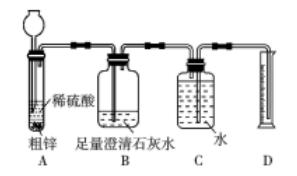
回答下列问题:
【查阅资料】
a、发热包内的粉末主要由生石灰、铁粉、铝粉、碳粉、氯化钠等组成;
b、铝是一种两性金属,与强酸、强碱溶液反应都能生成H2;
c、AgCl是既不溶于水又不溶于酸的白色沉淀。
【查阅资料】①Ag2O和粉末状的Ag均为黑色固体
②
③Ag2O可溶于氨水:Ag2O与稀硝酸反应生成AgNO3和H2O
④Ag不溶于氨水:
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1 常见草木灰钾含量(以碳酸钾表示)如下表:
草木灰种类 | 小灌木灰 | 稻草灰 | 小麦杆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
K2CO3(%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
2 提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。

【提出问题】该白色粉末的成分是什么?
【查阅资料】
①部分物质在水中的溶解性表(室温):
物质 | AgNO3 | AgCl | Ag2SO4 | AgCO3 |
溶解性 | 溶 | 不溶 | 微溶 | 不溶 |
②AgOH不稳定,在溶液中分解生成难溶于水的物质。

实验完毕后,小明误将A试管中的物质倒入B试管中,充分振荡后,观察到混合后溶液为无色。小明对该无色溶液的成分产生兴趣并展开探究(温馨提示:本题中番号①~⑤为答题卡上的序号)。
计算题