单选题(每小题3分,共45分)
试题详情
2023年5月28日,国产大飞机C919迎来商业首飞,C919机身部分采用第三代新型铝锂合金材料。下列关于铝和锂及合金的认识,正确的是( )
- A、 铝锂合金用于机身材料是因为密度较大,强度较大
- B、 多相R-Mg-Ni系储氢合金中,基态Ni原子中自旋状态相反的两种电子的个数比为13∶15
- C、 铝锂合金属于新型无机非金属材料
- D、 铝锂合金的性质保持了原来金属的性质,与各成分金属的性质都相同
试题详情
化学符号是化学学科进行思维的最基本的工具,下列微粒的化学符号表述正确的是( )
- A、 基态Zn原子的价层电子排布图:

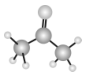
- B、 丙酮的球棍模型:
- C、 乙酸甲酯的结构简式:C3H6O2
- D、 NH3的电子式:

试题详情
设 为阿伏加德罗常数的值。下列说法中正确的是( )
为阿伏加德罗常数的值。下列说法中正确的是( )
- A、 常温下,pH为13的
溶液中含有
的数目为
- B、
溶液中含N的粒子数目为
- C、 粗铜精炼时,若阳极材料减少
, 电路中通过电子数一定为
- D、
%的甲酸水溶液中,含有的氧原子数为
试题详情
化学用语是学习化学最好的工具,下列化学用语能用于解释相应实验且书写正确的是( )
- A、 测得碳酸钠溶液呈碱性:
- B、 饱和
溶液滴入沸水中变红褐色:
- C、 铅酸蓄电池正极反应:
- D、 小苏打与明矾共溶于水,产生大量气泡:
↓
试题详情
我国科学家在世界上首次实现人工合成淀粉,下图是中间产物GAP的结构式,其中X、Y、Z、W均为短周期且原子序数依次增大的主族元素,且W的原子序数为其最外层电子数的3倍。下列说法正确的是( )
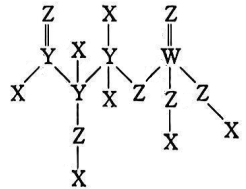
- A、 对应氢化物的沸点:Y<Z
- B、 X2Z2是由极性键和非极性键组成的非极性分子
- C、 W所在周期中,第一电离能比其小的元素有5种
- D、 1mol的该物质可以和足量的Na反应转移4mol的电子
试题详情
我国华中科技大学李钰团队研究了H2S在CuFe2O4催化剂表面吸附的历程,他们通过计算机模拟出的一种机理如图所示。

下列说法正确的是( )
- A、 CuFe2O4催化剂能降低该反应的焓变
- B、 决定该吸附历程速率的步骤是
- C、 吸附在催化剂表面的水分子解吸出来时放出能量
- D、 该吸附历程是H2S的分解过程
试题详情
高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料。它的发现和使用曾引起计算机的一场“革命”。可以按下列方法制备:
SiO2Si(粗)
SiHCl3
Si(纯)
下列说法不正确的是( )
- A、 步骤①的化学方程式为SiO2+C
Si+CO2↑
- B、 步骤①中每生成1 mol Si,转移4 mol电子
- C、 高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
- D、 SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏可提纯SiHCl3
试题详情
晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
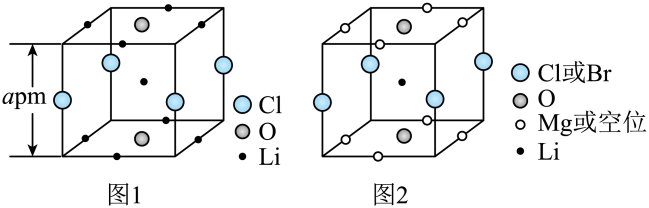
- A、 图1晶体密度为
g∙cm-3
- B、 图1中O原子的配位数为6
- C、 图2表示的化学式为
- D、
取代产生的空位有利于
传导
试题详情
室温下,下列实验探究方案能达到探究目的的是( )
选项 | 实验探究方案 | 探究目的 |
A | 向盛有Fe(NO3)2溶液的试管中滴加几滴稀硫酸,振荡,观察溶液颜色变化 |
|
B | 向溶液X中加入稀硫酸,并将产生的无色气体通入澄清石灰水中,观察是否有沉淀生成 | 溶液X中含有 |
C | 用pH试纸分别测定浓度均为0.1mol/L的NaCN和NaClO溶液的pH | |
D | 常温下,向10mL0.1mol/LNaCl溶液中滴加5滴0.1mol/LAgNO3溶液,充分反应后,再滴加5滴0.1mol/LKI溶液,观察沉淀颜色变化 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法错误的是( )
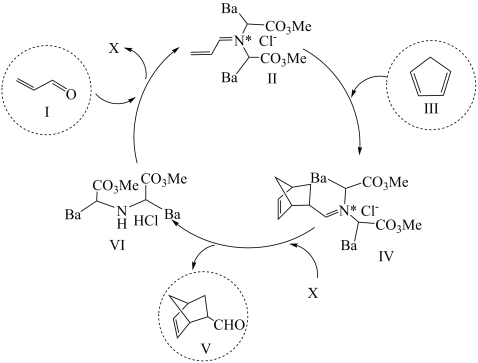
- A、 总反应为加成反应
- B、 Ⅰ和Ⅴ互为同系物
- C、 Ⅵ是反应的催化剂
- D、 化合物X为
试题详情
湖北蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一的结构简式如图。下列说法正确的是
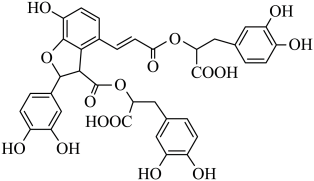
- A、 该物质属于芳香烃
- B、 可发生取代反应和氧化反应
- C、 分子中有5个手性碳原子
- D、 1mol该物质最多消耗9molNaOH
试题详情
我国科学家最近发明了一种 电池,电解质为
电池,电解质为 、
、 和KOH,通过a和b两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,结构示意图如下。下列说法不正确的是( )
和KOH,通过a和b两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域,结构示意图如下。下列说法不正确的是( )

- A、 a为阳离子交换膜、b为阴离子交换膜
- B、 电子由Zn电极经过外电路流向
电极
- C、 放电时,Zn电极反应为
- D、 消耗6.5gZn的同时,
电极理论上应增重3.2g
试题详情
在体积均为2L的恒容容器中,分别在200℃和T℃时,发生如下反应 , A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:
, A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
200℃ | 0.80 | 0.55 | 0.35 | 0.20 | 0.15 | 0.15 |
T℃ | 1.00 | 0.65 | 0.35 | 0.18 | 0.18 | 0.18 |
下列有关该反应的描述正确的是( )
- A、 在200℃时,4min内用B表示的化学反应速率为0.225mol/(L·min)
- B、 T℃下,6min时反应刚好达到平衡状态
- C、 从表中可以看出T>200℃
- D、 在该题目条件下,无法判断正反应方向是否为放热反应
试题详情
下图为 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(
关系图( ;
; 可认为
可认为 离子沉淀完全)。下列叙述正确的是
离子沉淀完全)。下列叙述正确的是

- A、 由
点可求得
- B、
时
的溶解度为
- C、 浓度均为
的
和
可通过分步沉淀进行分离
- D、
混合溶液中
时二者不会同时沉淀
实验题(12分)
试题详情
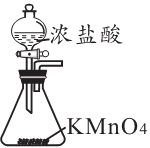
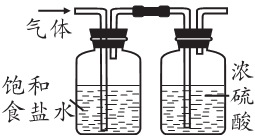
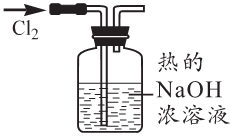
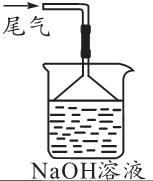
己二酸[HOOC(CH2)4COOH]是一种重要的工业原料,通常为白色结晶体,微溶于冷水,易溶于热水和乙醇。实验室以环己醇(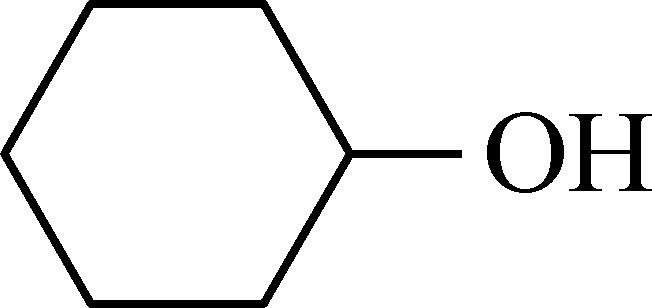 )为原料制取己二酸实验流程如图:
)为原料制取己二酸实验流程如图:
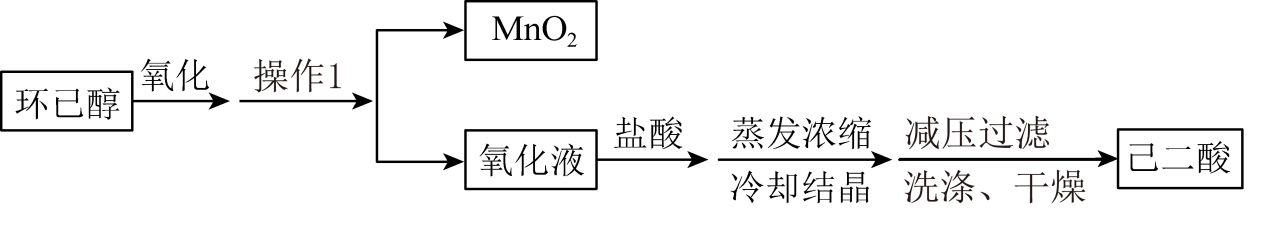
已知:“氧化”过程发生的主要反应为:![]()
KOOC(CH2)4 COOK △H<0
该反应装置如图所示。
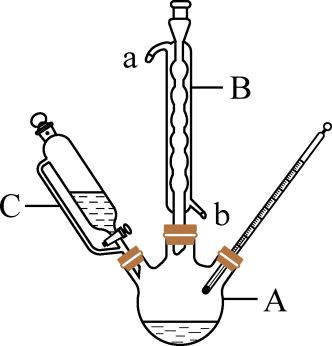
回答下列问题:
工业流程题(14分)
试题详情
锗是重要的半导体材料,是一种“稀散金属”,如图是以中和渣(主要成分为GeO2、Fe2O3、ZnO、SiO2、CaSO4等)为原料生产二氧化锗的工艺流程:
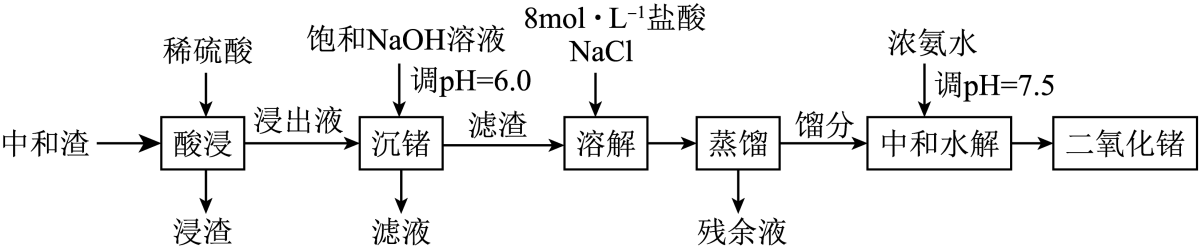
已知:
①GeCl4的沸点:83℃,FeCl3的沸点:315℃。
②H2GeO3在高酸度时易聚合形成胶状多聚锗酸。
③常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表(离子浓度低于10-5 mol·L-1视为沉淀完全)。
离子 | Fe3+ | Zn2+ |
开始沉淀pH | 2.2 | 6.2 |
完全沉淀pH | 3.2 | 8.2 |
回答下列问题:
原理综合题(14分)
试题详情
近年来我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将CO2转化为高附加值化学品成为科学家研究的重要课题。
有机推断题(15分)
试题详情
阿斯巴甜(G)是一种广泛应用于食品工业的添加剂,一种合成阿斯巴甜(G)的路线如下:
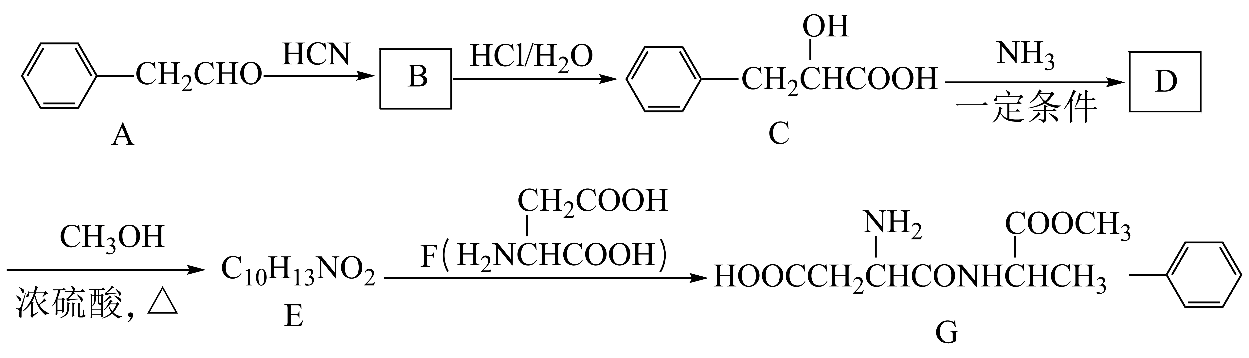
已知如下信息:
①![]()
![]()
②![]()
![]()
回答下列问题: