单选题
试题详情
下列各组反应中,不属于可逆反应的是
- A、 N2+3H2
2NH3和2NH3
N2+3H2
- B、 H2+I2
2HI和2HI
H2+I2
- C、 2H2+O2
2H2O和2H2O
2H2↑+O2↑
- D、 2SO2+O2
2SO3和2SO3
2SO2+O2
试题详情
可逆反应A(g)+4B(g)⇌C(g)+D(s),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
- A、 v(A)=0.15mol/(L·min)
- B、 v(B)=0.02mol/(L·s)
- C、 v(C)=0.4mol/(L·min)
- D、 v(D)=0.01mol/(L·s)
试题详情
一定温度下,浓度均为1 mol·L-1的A2和B2两种气体,在密闭容器中反应生成气体C,反应达到平衡后,测得:c(A2)=0.58mol/L,c(B2)=0.16mol/L,c(C)=0.84mol/L。则该反应的正确表达式为
- A、 2A2+B2⇌2C
- B、 A2+B2⇌2C
- C、 A2+B2⇌C
- D、 A2+2B2⇌2C
试题详情
X、Y、Z、W四种金属片在稀盐酸中,用导线连接,可以组成原电池,实验结果如图所示:则四种金属的活泼性由强到弱的顺序为

- A、 Z>Y>X>W
- B、 Z>X>Y>W
- C、 Z>Y>W>X
- D、 Y>Z>X>W
试题详情
类比推理是重要的学科思想,下列“类比”合理的是
- A、 Fe与S反应生成FeS,则Cu与S反应生成
- B、
与水反应生成
, 则
与水反应生成
- C、 Cu与浓
常温下反应生成
, 则Fe与浓
常温下反应生成
- D、 将蘸有浓氨水和浓盐酸的玻璃棒靠近会产生白烟,则将蘸有浓氨水和浓硫酸的玻璃棒靠近也会产生白烟
试题详情
下列陈述I、II均正确并且有因果关系的是
选项 | 陈述I | 陈述II |
A | SO2有漂白性 | SO2可使酸性高锰酸钾溶液褪色 |
B | NH3极易溶于水 | 充满NH3的试管倒置于水槽中,水面迅速上升 |
C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
D | 常温下,铁与浓硫酸发生钝化 | 常温下,铁与浓硫酸不反应 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
化学电源在日常生活和高科技领域中都有广泛应用,下列说法不正确的是
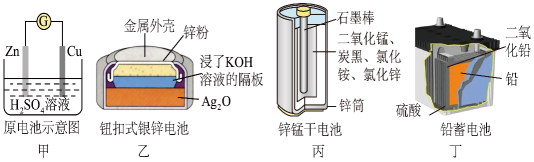
- A、 乙:正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
- B、 甲:溶液中Zn2+向Cu电极方向移动,电子由锌经电解质溶液流向铜电极
- C、 丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
- D、 丙:锌筒作负极,发生氧化反应,锌筒会变薄
试题详情
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是

- A、 反应开始到10s,用Z表示的反应速率为0.079 mol/(L•s)
- B、 反应开始到10s,X的物质的量浓度减少了0.79 mol/L
- C、 反应开始到10s时,Y的转化率为39.5%
- D、 反应的化学方程式为:X(g)+Y(g)=Z(g)
试题详情
用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是

- A、 上下移动①中铜丝可控制SO2的量
- B、 ②中选用品红溶液验证SO2的生成
- C、 ③中选用NaOH溶液吸收多余的SO2
- D、 为确认CuSO4生成,向①中加水,观察颜色
试题详情
下图为反应:H2(g)+Cl2(g)=2HCl(g)的能量变化示意图,下列说法正确的是

- A、 该反应每生成2molHCl,放出183kJ的热量
- B、 该反应生成液态HCl比生成气态HCl释放的能量少
- C、 氯气分子中的化学键比氢气分子中的化学键更稳定
- D、 1 molHCl分子中的化学键形成时吸收431kJ的能量
试题详情
在一密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1 , 当反应达到平衡时,可能存在的数据是
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1 , 当反应达到平衡时,可能存在的数据是
- A、 SO2为0.4 mol·L-1 , O2为0.2 mol·L-1
- B、 SO2为0.25 mol·L-1
- C、 SO2、SO3均为0.15 mol·L-1
- D、 SO3为0.4 mol·L-1
实验题
试题详情
为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
元素或物质推断题
试题详情
研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系如图。回答下列问题:

填空题
试题详情
某温度时,在一个2L的密闭容器中A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,回答下列问题:













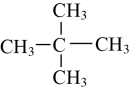 和
和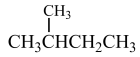 ⑥
⑥