单选题
- A、 自带布袋购物
- B、 草稿纸尽可能两面使用
- C、 使用一次性木筷
- D、 选择自行车作为出行工具
- A、 大量生产、使用能过滤PM2.5的口罩
- B、 对煤燃烧后形成的烟气进行尾气处理
- C、 开发利用太阳能、氢能、风能等清洁能源
- D、 研究廉价、高效的催化剂,以降低汽车尾气中有害物质的含量

- A、 钛是一种金属元素
- B、 核内中子数为22
- C、 元素符号为Ti
- D、 相对原子质量为47.87
- A、 镁条在空气中燃烧,发出耀眼的白光
- B、 细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
- C、 蜡烛在氧气中燃烧比空气里燃烧得更旺,发出白光
- D、 加热试管中的铜绿固体,绿色粉末逐渐变黑
- A、 Cr2O3
- B、 CrCl2
- C、 Cr2(SO4)3
- D、 K2CrO4
- A、 异黄酮中共含有17个原子
- B、 异黄酮的相对分子质量是222g
- C、 异黄酮中氧元素的质量分数最小
- D、 异黄酮由三种元素组成
- A、 应量取的水的体积为180mL
- B、 量取浓硫酸时仰视读数,则所得溶液的质量分数小于10%
- C、 实验中需要仪器有:烧杯、相应规格的量筒、胶头滴管、玻璃棒
- D、 装瓶时不小心洒漏一部分溶液,则瓶中硫酸溶液浓度小于10%
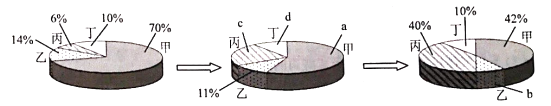
- A、 a=56%
- B、 b=6%
- C、 c=17%
- D、 d=8%
- A、 AgNO3固体应密封保存在无色细口瓶中
- B、 m=3.2
- C、 X的化学式为NO
- D、 该反应方程式中Ag与O2的化学计量数之比为3:2

- A、 40℃时,甲的溶解度大于乙的溶解度
- B、 20℃时,等质量的甲、乙溶液中溶质质量一定相等
- C、 将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液
- D、 将甲的饱和溶液转化为不饱和,溶质质量分数可能减小
多选题
| 物质 | 杂质 | 除去杂质的方法 | |
| A | NaCl固体 | 泥沙 | 溶解、过滤、洗涤、干燥 |
| B | CuSO4溶液 | H2SO4 | 加入足量的铜,过滤 |
| C | O2 | 水蒸气 | 通过足量的干燥剂 |
| D | 铜粉 | 锌粉 | 足量的稀硫酸,过滤、洗涤、干燥 |
填空题
XX牌高钙奶粉 配料表:脱脂乳、白砂糖、乳清蛋白、碳酸钙、硝酸亚铁、维生素A、维生素D等 | |
营养成分 | 每100g奶粉平均含量 |
能量 | 1733kJ |
蛋白质 | 18.2g |
磷 | 480mg |
钙 | 950mg |
铁 | 7.2mg |
A.氮气 B.石墨 C.稀有气体 D.武德合金 E.干冰 F.铜丝
实验题
图1 
图2 
流程题

计算题
科学探究题
(实验初探)①组装如图所示装置并检查气密性;②装入药品并固定;③加热一段时间后,B中固体颜色无明显变化,但吹泡器连续吹出气泡,且气泡向上飞起,用燃着的木条靠近气泡,能产生爆鸣。证明该气体为。

(查阅资料)常见的铁的氧化物有三种(FeO、Fe2O3、Fe3O4)
①三种氧化物中FeO、Fe3O4均为黑色;
①三种氧化物都不溶于水,其中铁粉、Fe3O4能被磁铁吸引
②三种氧化物都不与硫酸铜溶液反应,但能与酸反应生成可溶性物质。
(产物分析)实验小组同学对反应后玻璃管内的剩余固体进行探究。
①甲同学发现固体仍为黑色,由此判断:固体中肯定不存在Fe2O3 , 理由是。
②乙同学发现固体能全部被磁铁吸引,且黑色固体中一定没有。
(作出猜想)猜想I:全是Fe;猜想Ⅱ:全是Fe3O4;猜想Ⅲ:;
(定性探究)小组同学准确称取20g固体于试管中进行实验,加入过量溶液,出现红色固体,且有黑色固体残留。出现红色固体的化学方程式是,猜想成立,故铁与水蒸气发生置换反应的方程式是。
(定量测定)小组同学继续将上述定性探究实验后试管内的剩余物过滤、洗涤、干燥,称得固体质量为20.4g,则铁与水蒸气反应后玻璃管内固体中:剩余铁单质的质量为g(请写出此问解题过程),Fe3O4的质量分数为。
(实验反思)若定量测定中进行“干燥”操作时,将所得固体于空气中加热烘干,则会导致所得Fe3O4的质量分数(填“偏大”、“偏小”或“不变”)。

 混合
混合  成型
成型 晾干
晾干  烧结
烧结
 鉴别CO2、CO
鉴别CO2、CO  鉴别CO2、CO
鉴别CO2、CO 除去少量CO2
除去少量CO2  除去少量CO
除去少量CO




