单选题
试题详情
2022年1月14日,汤加火山喷发产生大量SO2进入大气。下列有关SO2说法正确的是( )
- A、 大气中SO2主要来源于火山喷发
- B、 SO2是直线形分子
- C、 食品中添加适量的SO2可以起到漂白和防腐等作用
- D、 可用盐酸酸化的BaCl2溶液检验气体中的SO2
试题详情
2021年我国科学家从一氧化碳到蛋白质一步合成的技术路线被突破。下列叙述不正确的是( )
- A、 CO是极性分子
- B、 工业上可用CO冶炼金属
- C、 新冠灭活疫苗的主要成分是蛋白质
- D、 蛋白质变性后均不能食用
试题详情
设NA为阿伏加德罗常数的值,下列说法正确的是( )
- A、 1molNH4F晶体中含有共价键数目为3NA
- B、 0.5molXeF4中氙的价层电子对数为3NA
- C、 标况下,11.2LNO和11.2LO2混合后的分子数目为NA
- D、 31g乙二醇中sp3杂化的原子数目为NA
试题详情
下列实验现象与实验操作不相匹配的是( )
实验操作 | 实验现象 | |
A | 向饱和溴化钾溶液中滴入氯化银饱和溶液 | 产生淡黄色沉淀 |
B | 向盛有乙苯的试管中滴加3滴酸性高锰酸钾溶液,振荡 | 紫色不褪去 |
C | 发黄的浓硝酸中通入O2 | 黄色变浅 |
D | 装有甲烷和氯气的试管置于光亮处 | 气体颜色变浅,试管壁有液珠 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
乙二醇生产工艺中,需使用热的K2CO3溶液(脱碳液)脱除CO2 , 脱碳液中含有的V2O5能减少溶液对管道的腐蚀。可使用“碘量法”测定脱碳液中V2O5的含量,操作中涉及两个反应如下:①V2O5+6HCl+2KI=2VOCl2+2KCl+I2+3H2O;②I2+2Na2S2O3=2NaI+Na2S4O6。下列说法不正确的是( )
- A、 反应①中氧化剂与还原剂物质的量之比为1:2
- B、 反应①生成1molVOCl2时,反应转移1mol电子
- C、 V的最高价为+5价,推测V2O5只有氧化性
- D、 溶液酸性过强时,反应②易发生其他反应
试题详情
由同周期元素原子W、X、Y、Z构成的一种阴离子(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20。下列说法正确的是( )
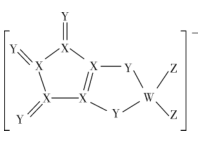
- A、 W、X、Y、Z第一电离能由大到小依次是:Z>Y>X>W
- B、 Y形成的简单离子的半径比Z形成的简单离子的半径小
- C、 W和X的最高价氧化物对应水化物的酸性:W>X
- D、 W、Z形成的化合物分子中各原子均满足8电子稳定结构
试题详情
某有机物的结构简式如图。下列有关该有机物的说法不正确的是( )
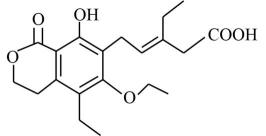
- A、 分子式为C20H26O6
- B、 既可以形成分子内氢键又可以形成分子间氢键
- C、 分子中有一个手性碳原子,具有一定的光学活性
- D、 1mol该有机物最多与3molNaOH反应
试题详情
下列关于元素及化合物的结构和性质的叙述正确的是( )
- A、 稳定性:H2Se<H2S<H2O,三者都是V形分子
- B、 SO3和H2SO4中的硫原子都采取sp3杂化
- C、 P4分子和
离子中的键角都为109°28ˊ
- D、 F2能与NaCl溶液反应置换出Cl2
试题详情
砷化镉晶胞结构如图。图中“①”和“②”位是“真空”,晶胞参数为apm,建立如图的原子坐标系,①号位的坐标为( ,
,  ,
,  )。已知:砷化镉的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值。下列说法不正确的是( )
)。已知:砷化镉的摩尔质量为Mg/mol,NA为阿伏加德罗常数的值。下列说法不正确的是( )

- A、 砷化镉中Cd与As原子个数比为3:2
- B、 两个Cd原子间最短距离为0.5apm
- C、 ③号位原子坐标参数为(
, 1,
)
- D、 该晶胞的密度为
g·cm-3
试题详情
制备苯甲酸甲酯的一种反应机理如图(其中Ph-代表苯基)。下列说法不正确的是( )
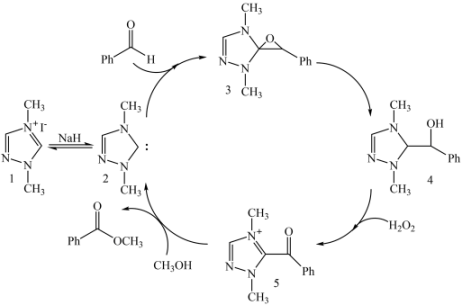
- A、 化合物2到化合物3的过程,存在极性键的断裂和生成
- B、 化合物4到化合物5的过程,H2O2体现了还原性
- C、 苯甲酸甲酯分子中所有C和O原子可能共平面
- D、 制备苯甲酸甲酯的化学方程式:
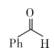 +H2O2+CH3OH
+H2O2+CH3OH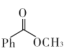 +2H2O
+2H2O
试题详情
在一定温度下,BaSO4和C在一密闭容器中进行反应:BaSO4(s)+4C(s) BaS(s)+4CO(g),CO的平衡浓度(mol/L)的对数lgc(CO)与温度的倒数
BaS(s)+4CO(g),CO的平衡浓度(mol/L)的对数lgc(CO)与温度的倒数 的关系如图所示,下列说法中正确的是( )
的关系如图所示,下列说法中正确的是( )
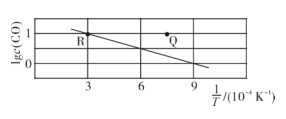
- A、 Q点BaSO4的消耗速率小于生成速率
- B、 该反应的ΔH<0
- C、 温度是
K时,反应的平衡常数为1
- D、 温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
试题详情
以赤铁矿(主要成分为Fe2O3 , 含少量Al2O3)为原料制备无水FeCl2的工艺流程如下。下列说法不正确的是( )
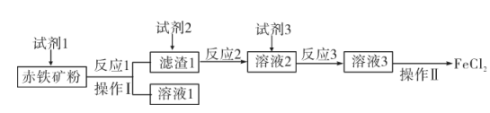
- A、 试剂1可用NaOH溶液
- B、 鉴别溶液2中金属阳离子可用KSCN溶液
- C、 反应3为化合反应
- D、 将溶液3蒸干可制得无水FeCl2
试题详情
可用惰性电极通过电解法制备KMnO4 , 下列说法正确的是( )
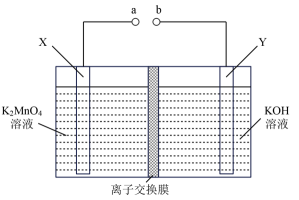
- A、 图中离子交换膜为阴离子交换膜
- B、 X极的电极反应为MnO
-e—=MnO
- C、 Y极区可以产生O2和较浓的KOH溶液
- D、 电解一段时间后阴极区溶液的pH减小
试题详情
室温下,向100mL某浓度的二元弱酸H2A溶液中逐滴加入0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如图所示。下列有关说法不正确的是( )

- A、 Ka1(H2A)数量级为10-3
- B、 b点时:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
- C、 水的电离程度:d>c>b>a
- D、 b→c段,反应的离子方程式为HA-+OH-=A2-+H2O
综合题
试题详情
钼酸钠(Na2MoO4)是一种冷却水系统的金属缓蚀剂,工业上通常利用钼精矿(主要成分MoS2中硫为-2价)制备钼酸钠晶体的流程如图所示。
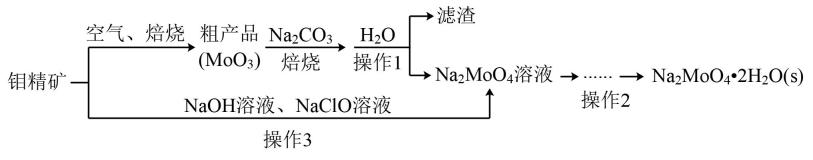
回答下列问题:
试题详情
有机物E是合成药物的中间体,E的合成路线如下:
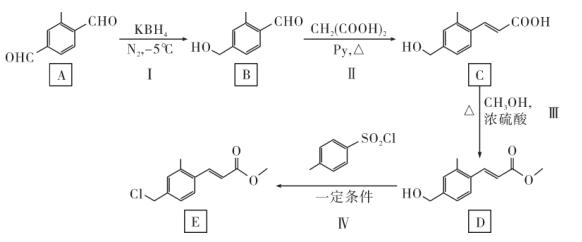
回答下列问题:
试题详情
磺酰氯(SO2Cl2)可用于制造锂电池正极活性物质。实验室可利用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2 , 装置如图(部分夹持装置已省略)。
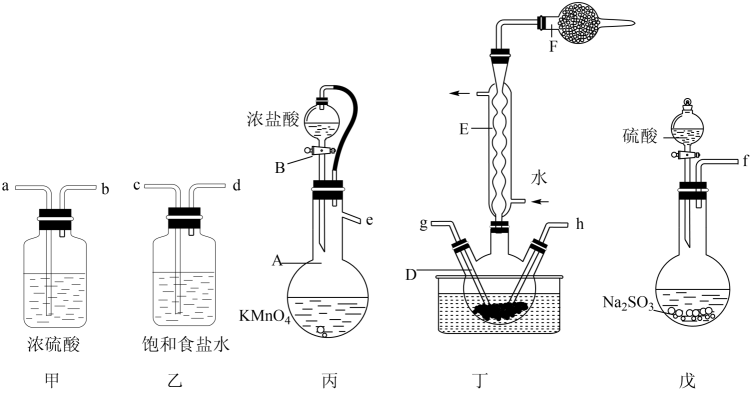
已知:①SO2(g)+Cl2(g)=SO2Cl2(1) △H=-97.3kJ/mol。
②SO2Cl2熔点为-54.1℃,沸点69.1℃,常温较稳定。遇水剧烈水解,100℃以上易分解。
回答下列问题:
试题详情
研究碳及其化合物的资源化利用具有重要的意义。回答下列问题: